|
Утилизация углекислоты при производстве спирта
При брожении осахаренной массы крахмала и сахарсодержащего сырья в герметически закрытых бродильных аппаратах выделяются газы, которые являются почти чистой углекислотой: содержание углекислоты в них составляет 99—99,5%. Процесс выделения углекислоты протекает по уравнению: С6Н12О6 = 2С2Н5ОН + 2СО2 Сахар Этиловый спирт Углекислый
Выход углекислоты составляет 95,5% от веса спирта, 51,3% — от веса сахарозы и 54,2% — от веса крахмала. Принимая в среднем выход спирта равным 90,3% от теоретического, что составляет 65,0 дал из 1 тонны крахмала, получим расчетный выход углекислоты, равный 7,53 кг на 1 дал полученного спирта, или 48,95 кг углекислоты на 1 тонну переработанного крахмала. Практически степень использования углекислоты при переработке зерно-картофельного сырья может составлять примерно 70% от общего ее выхода, так как при наполнении бродильных аппаратов углекислота смешивается с воздухом. При непрерывном процессе сбраживания с постоянным притоком газ не смешивается с воздухом и может быть использован почти полностью. При переработке мелассы используется только 50% углекислоты, выделяющейся в дрожжегенераторах, так как она также разбавлена воздухом. Выход углекислоты в зависимости от вида перерабатываемого сырья приводится в табл. 1. Таблица 1
В качестве примесей в выделяющейся при брожении углекислоте обнаруживаются спирт (0,4—0,8% по весу СО2), эфиры (0,03—0,4%), кислоты (0,08—0,09%) и следы альдегидов. После несложной очистки из этого газа можно получить пищевую, почти химически чистую углекислоту в виде товарной жидкой или (твердой) сухой углекислоты или потреблять на месте в газообразном состоянии.
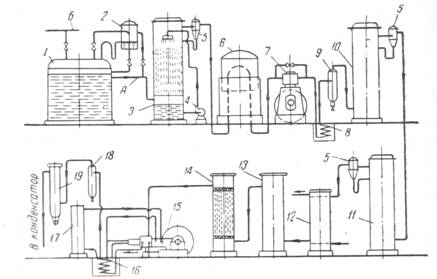
Производство жидкой углекислоты. Получение жидкой пищевой углекислоты из газов брожения на спиртовых и пивоваренных заводах ведется по схеме, изображенной на рис. 3. Углекислый газ, выделяющийся при брожении из герметически закрытых бродильных чанов /, снабженных гидравлическими предохранителями, направляется в спиртоловушку 2 для промывки и освобождения от продуктов брожения. Во время очередного заполнения каждого бродильного чана воздух вместе с начавшим выделяться углекислым газом отводят в атмосферу; как только остаток воздуха будет вытеснен выделяющимся газом, чан подключают к сборному газопроводу. Углекислый газ, проходя гидравлическую спиртоловушку, направляется в холодный скруббер 5, орошаемый водой при помощи насоса 4; здесь происходит предварительная промывка и удаление из газа эфиров, альдегидов, высших спиртов, сивушных масел и других побочных продуктов спиртового брожения. Очищенная в скруббере углекислота через брызгоуловитель 5 нагнетается вентилятором в сборник газа — газгольдер 6. Из газгольдера углекислый газ, проходя грязевик, поступает под давлением 0,1 ати во всасывающую линию первой ступени сжатия трехступенчатого углекислотного компрессора, где он сжимается до давления 4,5 ата, вследствие чего температура его повышается до 100°С. Сжатие необходимо для того, чтобы газ мог преодолеть значительные сопротивления в последующих фильтрах. После первой ступени сжатия углекислый газ подвергается тщательной очистке от различного рода оставшихся в нем примесей и охлаждению до температуры 25 °С. До поступления в очистительную батарею СО2 проходит маслоотделитель (для улавливания могущих попасть от компрессора взвесей масла) и холодильник для охлаждения, после чего направляется на очистку. Очистительная батарея состоит из последовательно соединенных цилиндрических резервуаров — фильтров, заполненных — 1 %-ным раствором перманганата калия — для окисления органических примесей газа; : двух, поочередно работающих,
одного — водой — для отмывки газа от примесей других газов и остатков побочных продуктов брожения; одного — хлористым кальцием, осушающим углекислоту (удаляющим влагу), и двух, поочередно работающих, заполненных активированным углем для очистки углекислоты от различного рода могущих быть в ней запахов.
Рис. 3. Схема производства жидкой СО2 из углекислоты брожения: А - общий газовый трубопровод; Б — трубопровод в атмосферу. Затем газ направляется последовательно во вторую и третью ступени сжатия и оттуда поступает на розлив в баллоны или для получения сухого льда. Из газгольдера 6 газ засасывается и сжимается до 1 — 1,5 ати одноступенчатым воздушным компрессором 7. Сжатый газ, пройдя промежуточный охладитель 8 и маслоотделитель 9, нагнетается для очистки последовательно в колонну с раствором марганцевокислого калия 10 и колонку с раствором соды 11. Далее газ охлаждается в холодильнике газа 12 и поступает для сушки в колонку, наполненную безводным хлористым кальцием или силикагелем 13. После осушки газ поступает для окончательной очистки в колонку с активированным углем 14, после чего направляется в трехступенчатый углекислотный компрессор15 для сжатия и сжижения. Во второй ступени компрессора газ сжимается до 18—20 ати, при этом давлении, пройдя промежуточный охладитель 16 и колонку с хлористым кальцием 17, он поступает на третью ступень компрессора, где сжимается до 60—70 ати в зависимости от температуры охлаждающей воды. Далее газ проходит маслоотделитель 18 и поступает на фильтр с силикагелем 19 и углекислотный конденсатор, оттуда сжиженная углекислота направляется в наполнительно-весовую станцию для разлива в баллоны. Колонки с хлористым кальцием или силикагелем и активированным углем целесообразно сдваивать, чтобы проводить их перезарядку без нарушения процесса очистки углекислоты. Приведенная схема получения углекислоты целесообразна для крупных заводов; на небольших предприятиях очистительную аппаратуру можно устанавливать после первой и второй ступеней сжатия трехступенчатого углекислотного компрессора. Получение сухого льда. Для получения твердой углекислоты жидкость направляется в испаритель, где часть ее улетучивается, а остаток превращается в снегообразную массу (сухой лед), которая спрессовывается в твердое тело. Производство и потребление жидкой углекислоты связано с организацией баллонного хозяйства (емкостей) из стальных баллонов, работающих под высоким давлением и предназначенных для наполнения, хранения, перевозок и расходования углекислоты. Стальные баллоны для жидкой углекислоты нуждаются в постоянном техническом надзоре и систематическом ремонте для поддержания в работоспособном и безопасном состоянии. Организация и содержание многочисленного сложного и дорогостоящего баллонного хозяйства требует больших затрат труда и расход на нее составляет свыше 30% к общему размеру капитальных вложений на ввод в действие новых мощностей для производства жидкой углекислоты. Углекислота в тяжелых стальных баллонах старого типа малотранспортабельна, так как вес баллонной тары составляет 70% при весе продукта 30% и для перевозки 1 тонны углекислоты потребители вынуждены перевозить в оба конца 4,5 тонны тары ( В баллонах нового типа с меньшим излишком запаса прочности и значительно уменьшенным весом (выпуск таких баллонов начат с 1958 г. соотношение веса тары и продукта несколько лучше, но все же вес тары в 1,5 раза превышает вес продукта). Перевозят жидкую углекислоту в основном дорогим автомобильным транспортом, так как углекислота отнесена МПС к категории опасных грузов, перевозки которых железнодорожным транспортом регламентированы и потому, естественно, ограничиваются. При таких условиях себестоимость жидкой углекислоты для потребителей резко удорожается за счет высоких транспортных и накладных расходов, достигающих в ряде случаев 100% и более к оптово-отпускной цене франко-склад завода. Стоимость перевозок жидкой углекислоты даже на короткие расстояния составляет в среднем 30—40% к ее общей покупной стоимости. Хранение и расходование взрывоопасной жидкой углекислоты регламентированы определенными техническими правилами, обеспечивающими безопасность работы, но требующими дополнительных затрат труда и денежных средств. Недостаток баллонной тары ограничивает размеры производства жидкой углекислоты, особенно в межсезонный период. Указанные причины способствовали усиленному развитию за последние годы за границей, особенно в США и Англии, практики сжижения сухого льда с получением в пунктах потребления в необходимых случаях жидкой или газообразной углекислоты. Сухой лед при сжижении дает углекислый газ 100%-ной чистоты, не требует при перевозке тары, рассчитанной на высокое давление, поэтому и стоимость перевозок его намного ниже. Хранилище для сухого льда. В связи с низкой температурой (минус 78,9°С) сухой лед воспринимает тепло окружающей среды и сублимируется (испаряется). Скорость сублимации и связанные с нею размеры потерь сухого льда. прямо пропорциональны разности температур между сухим льдом и окружающей его средой. Поэтому для хранения сухого льда создают герметически закрытые, заглубленные в землю хранилища с плотной надежной изоляцией толщиной до 300 мм. Наружные стены и днище такого хранилища выполняют из листовой стали, а швы между листами пропаивают. Внутри хранилище для сухого льда разделяют на отдельные отсеки перегородками из изоляционного материала. В каждый отсек вставляется этажерка для укладки в нее блоков сухого льда. Этажерка опускается при загрузке сухого льда и поднимается при выгрузке его с помощью электротельфера. Загрузка и выгрузка сухого льда проводится через верхние люки льдохранилища, снабженные крышками с высококачественной плотной изоляцией. По емкости льдохранилище рассчитывается минимально на двухсуточную производительность или потребность. Размеры потерь сухого льда при хранении зависят от степени загрузки хранилища, так как при сублимации образуется своеобразный защитный слой газообразной углекислоты. Льдохранилище описанного типа с верхней загрузкой блоков сухого льда представлено на рис. 4. Для перевозки твердой углекислоты Институтом холодильной
промышленности разработана конструкция деревянных контейнеров емкостью 1600,
1000, 500 и Использование естественной углекислоты, получаемой в процессах брожения, является наиболее экономически рентабельным способом производства товарной углекислоты.
Рис. 4. Хранилище для сухого льда. Такое производство сухого льда не требует расходования на эти цели исходного сырья, а также довольно сложного и металлоемкого оборудования, как на специальных углекислотных заводах, получающих СО2 из дымовых газов сжигаемого кокса или антрацита. Для выработки 1 тонны жидкой углекислоты из газов брожения
расходуется 190 квт-ч электроэнергии, в
то время как на специализированных углекислотных заводах — 175 квт-ч электроэнергии, 750—850 кг антрацита
и Расчеты показывают, что при правильном использовании газов брожения, улучшении организации производства и труда в углекислотных цехах спиртовых заводов себестоимость жидкой углекислоты может быть значительно снижена. Промышленное использование отходящей углекислоты спиртового брожения возникло в годы первой
пятилетки. Первый углекислотный цех был оборудован на Мироцком
спиртовом заводе в Спиртовые заводы с углекислотными цехами заняли ведущее место в углекислотной промышленности страны, составляя по численности 34% и по производительности 37% всех предприятий, вырабатывающих углекислоту. На спиртовых заводах вырабатывается более 25% производимой в СССР углекислоты. Общее число предприятий, использующих углекислоту спиртового брожения спиртовых и пивоваренных заводов, составляет 47% всех мощностей по производству углекислоты, в то время как в США удельный вес предприятий, использующих углекислоту брожения, равен 43%. Однако общее использование СО2 на спиртовых заводах крайне незначительное — всего 4,5% от возможного выхода товарной углекислоты. На спиртовых заводах ежегодно выбрасывалось в атмосферу до 1 млн. т углекислоты, в том числе по УССР — до 180 тыс. т. Так, например, даже на крупных спиртовых заводах, имеющих углекислотные установки, использование углекислоты в свое время было весьма низкое, что видно из данных табл. 2. Таблица 2
На крупных заводах США, перерабатывающих спирт, углекислоту перерабатывают на сухой лед. Вопросу эффективного использования углекислоты брожения на спиртовых заводах должно быть уделено особое внимание. Необходимо оборудовать углекислотные цехи в первую очередь на спиртовых заводах Урала, Сибири, Дальнего Востока, Казахстана и Украины, где ощущается недостаток в углекислоте.
В пищевой промышленности углекислота используется для: производства безалкогольных напитков, минеральных вод, пива, сидра и газированных соков. Предприятия пищевой промышленности потребляют 38% всей вырабатываемой углекислоты. В промышленности, на транспорте и в строительстве углекислота используется для приготовления газированной воды в горячих цехах. Она также применяется для наполнения противопожарного оборудования. Углекислота приобретает особое значение в литейном деле при изготовлении форм и стержней на смесях с жидким стеклом способом химического твердения с продувкой их углекислым газом. Кроме того, углекислота используется для подкормки выращиваемых в теплицах овощей. В последнее время разработан метод сварки газопроводов в среде углекислоты, что позволяет вести сварку труб без шлаковых включений и получать швы высокого качества. На мясокомбинатах углекислота применяется для предубойного оглушения свиней в заполненном углекислым газом туннеле. В результате пребывания животного в атмосфере СО2 (60%) в течение 30 сек достигается состояние анестезии, продолжающееся около 4 мин. По семилетнему плану на ряде спиртовых заводов намечено оборудование цехов для выпуска жидкой и твердой углекислоты. В развитие этого плана в 1960—1961 гг. на Корыстовском и Шадринском спиртовых заводах оборудованы углекислотные цехи производительностью по 5 т жидкой углекислоты в сутки и вводятся в действие установки для выработки более 2 т сухого льда в сутки. Получение из углекислоты углекислого аммония (карбоната аммония). Как указано выше, лишь незначительная часть выделяющейся при брожении СО2 используется для сжижения (3—5%) - Основное количество СО2 выбрасывается в атмосферу. Разработан способ использования отходящей углекислоты брожения для получения углекислого аммония. Углекислота связывается с аммиаком, применяемым в виде аммиачной воды 15%-ной концентрации. При этом получается 40%-ный раствор углекислого аммония. Реакция образования углекислого аммония из углекислоты и аммиака: NН4ОН + СО2 = (NН4)2СО3 + Н2О протекает быстро при нормальном давлении и температуре.
По этому уравнению из 1 тонны углекислоты можно получить 2,17 тонн углекислого аммония (карбоната аммония). При непрерывной циркуляции угольной кислоты через раствор около 10% СО2 выводят из цикла во избежание накопления инертных газов, главным образом воздуха. Таким образом, фактически из 1 тонны СО2 получится 2 тонны углекислого аммония (карбоната аммония), или 5 тонн раствора 40% -ной концентрации. Расход аммиака в виде 25%-ного раствора аммиачной воды составляет с учетом потерь 0,62 тонны на 1 грамм 40%-ного углекислого аммония. Получаемый продукт представляет собой бесцветную, слегка
мутноватую жидкость уд. веса
1,13 с содержанием в Суточная норма дачи 40%-ного раствора углекислого аммония (карбоната аммония) составляет (в мл): · крупному рогатому скоту ........... 430 · молодняку крупного рогатого скота ...... 220 · овцам и козам ................ 30
Применение углекислого аммония в качестве заменителя азота белка в
кормовых рационах для жвачных животных весьма эффективно. По данным проф.
Панова, добавки в кормовые бедные белком рационы углекислого аммония обеспечили
повышение привеса животных на Молодняку крупного рогатого скота на откорме требуется в сутки 600 г переваримого протеина. Из этого количества 25%, т. е. 150 г, может быть заменено азотом углекислого аммония. Это составит При такой норме каждые 0,25 кг раствора углекислого аммония дают повышение привеса в 0,121 кг. Продукция установки производительностью 5 тонн раствора в сутки при откармливании молодняка крупного рогатого скота дает суточное повышение привеса в количестве: 5000 Х 0,121 / 0,25 Х 1000 = 2,42 тонн мяса
По содержанию азота 1 кг раствора углекислого аммония равен 0,72 кг белка, или, с учетом коэффициента переваримости, 1 кг раствора эквивалентен 0,58 переваримого протеина. По данным Института животноводства, при кормлении молочных коров на образование 1 кг молока требуется 1 кормовая единица при нормальном рационе (85—95 г белка на 1 кормовую единицу). При недостатке белка в рационе (50 — 60 грамм на 1 кормовую единицу) расход корма увеличивается до 1,5 — 2,0 кормовых единиц на 1 кг молока. Восполнение недостающего белка в рационах раствором позволит сэкономить корм. 213 На 1 кормовую единицу требуется добавить 30 грамм белка до нормы или ~52 грамма раствора углекислого аммония, что сберегает 0,7 кормовых единиц, или 0,7 кг зерна (овса). Использование в животноводстве 5000 тонн раствора соли аммония в сутки экономит 50 тонн зерна. По данным Института Аскания-Нова, на образование 1 кг шерсти овец требуется от 80 до 100 кормовых единиц с содержанием не менее 80—85 грамм белка на 1 к.е. (кормовую единицу). При недостатке 30% белка расход корма составляет 160 к.е. и больше, а настриг шерсти падает. Добавление в рацион овец раствора углекислого аммония в количестве 51 г на каждую кормовую единицу позволит восполнить недостающий азот белка в рационе до нормы и сохранить недополученный из-за недостаточности белка в корме настриг шерсти в количестве 1,25—1,50 кг. На образование этой шерсти затратится всего: 51 Х 600 / 1000 =
Тогда суточная продукция установки (5 т) при использовании в животноводстве может обеспечить привес шерсти в количестве 205—246 кг. Особенно эффективно применение углекислого аммония при скармливании силоса, в том числе кукурузного. Скармливание кислых силосованных кормов часто вызывает воспаление пищеварительного тракта животных. Вследствие этого очень часто применяется подщелачивание силосованных кормов мелом или щелочами, что не изменяет питательной ценности корма. Если же для нейтрализации силосованных кормов применять раствор углекислого аммония, то он быстро и полностью нейтрализует молочную кислоту с образованием молочнокислого аммония, который является хорошим заменителем белка. Следовательно, добавление углекислого аммония к силосу нейтрализует кислоты и одновременно обогащает силос белком. Питательность силоса резко возрастает и он превращается в белковый корм, который так необходим животным. Применение углекислого аммония весьма эффективно при силосовании сахаристых кормов и кормов, содержащих большое количество углеводов. При силосовании таких кормов происходит быстрое накопление молочной кислоты и снижается рН; жизнедеятельность молочнокислых бактерий подавляется и дальнейшее образование молочной кислоты прекращается, хотя в силосе остается еще значительное количество сахара, вследствие чего ухудшается сохраняемость такого силоса. Однако если в процессе силосования, который длится 10 — 20 дней, добавлять раствор углекислого аммония, то можно постепенно нейтрализовать образующуюся молочную кислоту. Процесс закисания будет происходить беспрепятственно до тех пор, пока все углеводы не превратятся в молочную кислоту. Молочная кислота дает молочнокислый аммоний и силос будет богат хорошем заменителем белка и по существу превратится в высшей степени питательный белковый концентрат. Получение углекислого аммония осуществляется по схеме (рис.5). 25%-ная аммиачная вода поступает на завод в железнодорожных цистернах емкостью 25 или 50 тонн и направляется в хранилище 1. Хранилище емкостью 25—50 тонн расположено на открытом воздухе.
Рис. 5. Схема установки для непрерывного получения углекислого аммония в жидком виде.
Из хранилища аммиачная вода центробежным насосом 8 качается в сборник аммиачной воды 2, расположенный в цехе. Емкость сборника рассчитана на 8-часовую работу установки. Из сборника аммиачная вода через дозатор 4 поступает в сатуратор 9, перед которым она смешивается с водой, поступающей из ловушки аммиака 3. Вода разбавляет аммиачную воду до концентрации 14,6%. Углекислота из бродильного цеха отсасывается воздуходувкой 11, сжижается до давления 0,3—0,6 ати и подается в сатуратор через барботер. Отходящая углекислота отводится из сатуратора в верхней его части и натравляется в брызгоулавливатель 5 — цилиндрический сосуд с наклонно поставленными полками. Пройдя брызгоулавливатель, углекислота отводится, соединяется со свежей углекислотой и насосом подается опять в сатуратор. Небольшое количество газов (10%) выводится периодически из цикла. Отходящие газы проходят ловушку 3, где происходит улавливание аммиака водой. Ловушка представляет собой цилиндрический сосуд с коническим днищем. Внутри ловушки имеется насадка из колец Рашига. Ловушка непрерывно орошается водой, которая затем используется для разбавления 25%-ной аммиачной воды. Готовый раствор с содержанием 40% углекислого аммония непрерывно отбирается из сатуратора через декантатор 6, где происходит отделение раствора от газа. Выделившаяся из раствора углекислота отводится обратно в сатуратор. Раствор углекислого аммония из декантатора поступает в сборник 10 и затем, по мере его заполнения, готовый продукт перекачивается в хранилища 7. Установка для производства углекислого аммония несложна. Стоимость оборудования цеха производительностью 5 тонн раствора углекислого аммония в сутки составляет 9 тыс. руб. Стоимость азота углекислого аммония, вырабатываемого на спиртовом заводе, в 2 раза дешевле азота мочевины и почти одинакова со стоимостью азота бикарбоната, выпускаемого химической промышленностью. Отсюда следует, что организация таких цехов на спиртовых заводах весьма рентабельна.
Смотри также: Аппараты для производства жидкой углекислоты ( CO2 ) из газов брожения
На спиртовом заводе мощностью 1000 дал спирта в сутки выделяется ежедневно 7 тонн углекислоты, из них может быть получено около 15 тонн углекислого аммония. Представляется целесообразным организовать производство углекислого аммония в первую очередь на тех спиртовых заводах, которые без особых затруднений могут получать аммиачную воду с ближайших предприятий. В настоящее время введены в действие установки для получения углекислого аммония на Пронском и Лужковском спиртовых заводах. Применение углекислоты для перемешивания бражки. На ряде спиртовых заводов (Корыстовском, Спасо-Сергиевском и др.) с 1955 г. применяется способ перемешивания бражки и дрожжей углекислым газом (рис. 6). Углекислый газ, освобожденный от спирта специальным компрессором, направляется в сборник-ресивер, где поддерживается давление 3 — 3,5 атм. Из ресивера углекислый газ поступает в барботеры, установленные в нижней части бродильного чана, вызывая при этом энергичное перемешивание бродящей массы. Перемешивание углекислым газом проводится 3 раза до начала главного брожения, а именно: по заполнении 1/3 чана, 1/2 чана и после полного заполнения, а по истечении 36 часов от начала заполнения чана — через каждые 5 часов до конца брожения. По исследованиям С. П. Гуляева, благодаря созданию анаэробных условий сбраживания при перемешивании бродящей среды СО2 накопление биомассы дрожжей уменьшается на 15—30%, а количество несбраживаемых сахаров — на 30—40%; продолжительность брожения сокращается на 6—8 часов. По данным А. Б. Козареза, расход СО2 на перемешивание составляет 1 баллон на бродильный чан емкостью 8000 дал (80 000 литров или 80 м3).
Рис.6. Схема перемешивания углекислым газом содержимого бродильных чанов и дрожжанок на Корыстовском спиртовом заводе: / — бродильные чаны; 2 — дрожжанки; 3 — спиртовая ловушка, 4 — ресивер; 5 — компрессор. Использование углекислого газа в сельском хозяйстве. В последнее время уделяется большое внимание использованию газового удобрения в сельском хозяйстве. В процессе фотосинтеза растения усваивают из воздуха углекислый газ и преобразуют неорганические минеральные вещества в органические. Однако содержание углекислого газа в атмосфере — около 5 г/м3, или 0,03% по объему, недостаточно для фотосинтеза. Для восполнения недостатка углекислого газа применяют газовое удобрение. По данным Константинова, использование углекислого газа в качестве удобрения на свекловичных участках повысило урожайность свеклы на 27%, а содержание сахара в ней увеличилось на 1,03—1,45%. В оранжереях и теплицах прибавление углекислого газа увеличивает урожайность на 100—150%. На некоторых спиртовых заводах углекислый газ брожения отводится в теплицы, расположенные близ заводов. В эти теплицы в холодное время года подается теплая вода по трубопроводу, который в теплое время используется для подвода углекислого газа. Как показал опыт теплиц Мартыновского спиртового завода, при поливке водой, насыщенной углекислым газом, урожайность овощей значительно повысилась. Углекислый газ по трубопроводам с помощью
компрессора может быть транспортирован и на колхозные поля. При этом спиртовый завод производительностью 1000 дал спирта в сутки
может обеспечить ежесуточным газовым удобрением
Собственное производство азотного удобрения
Атмосфера Земли на 78% состоит из азота N2 ,остальное - кислород и прочие газы. Азот входит в состав ископаемых углей и торфа. Азот в соединении с углеродом, водородом и кислородом образует белковые вещества, которые входят в состав растительных и животных организмов и составляют основу жизни. O2 Растения не усваивают ни свободный азот, ни азот, входящий в состав сложных органических веществ. Растения избирательно извлекают необходимые элементы из водного почвенного раствора неорганические соединения в виде ионов (катионов NH4+, K+, Mg2+, Ca2+, H+ и анионов NO3-, H2PO4-, SO42- и других). C выращенными продуктами в современном сельском хозяйстве уносится азота больше, чем восполняется природными процессами и вносится в почву человеком. При недостатке азота рост растений задерживается, листья желтеют и опадают, процесс фотосинтеза заканчивается. Внесение удобрений является одним из важнейших агротехнических мероприятий, обеспечивающих высокие урожаи. Хорошо растворимые азотные удобрения, особенно нитраты, вымываются из почвы. Некоторая доля азота под действием микроорганизмов восстанавливается из иона ΝО3 - до Ν2 и Ν2О и улетучивается в атмосферу (денитрификация). Поэтому минеральный азот в почве практически не накапливается и его необходимо вносить в больших количествах. Темпы роста производства минеральных (искусственных) азотных удобрений чрезвычайно высоки.
Данные: Аммиачная вода (Аммиак водный технический марки А, Б ГОСТ 9-92) в железнодорожных цистернах Углекислый газ (Двуокись углерода ГОСТ 8050-85) в автомобильных цистернах Гипс
1 Вариант. Карбонат аммония
NH4OН + CO2 → (NH4)2CO3 + Н2O Аммиачная вода Углекислый газ Карбонат аммония Вода 18,04 44,01115 96,09115 18,016
Кристаллы карбоната аммония Карбонат аммония - кристаллы белого, серого или розового цвета. Хорошо растворим в воде. В Российской Федерации - ТУ 2144-007-05761637-2006. Очень неустойчив как на воздухе, так и в растворе, так как уже при комнатной температуре выделяет аммиак, превращаясь в бикарбонат аммония NH4HCO3. При t 60 °C быстро распадается на NH3, CO2 и H2O. Подвергается гидролизу: (NH4)2CO3 + H2O = NH4OH + NH4HCO3. В пищевой промышленности классифицируются как эмульгаторы. Карбонат аммония имеет массовую долю аммиака (NH3) не более 20,7% 2 Вариант. Сульфат аммония
Сульфат аммония получают обрабатывая гипс растворами карбоната аммония (NH4)2CO3 + CaSO4 → (NH4)2SO4 + CaCO3 Карбонат аммония Гипс Сульфат аммония Известь 96,09115 136,146 132,146 100,09115 Сульфат аммония (сернокислый аммоний), формула (NH4)2SO4- азотно-серное минеральное удобрение (в Российской Федерации — ГОСТ-9027-82). Сульфат аммония содержит 21 % азота и 24 % серы. Это химически нейтральная кристаллическая соль белого цвета, хорошо растворимая в воде. Гигроскопичность её слабая, поэтому при длительном хранении не слёживается и сохраняет сыпучесть. Азот и сера — важнейшие элементы питания сельскохозяйственных культур: они входят в состав белков и аминокислот. В последние годы наблюдается тенденция снижения содержания серы в пахотных почвах во многих регионах России, около 80% пашни бедны серой. Наличие в составе сульфата аммония серы, положительно влияющей на качество сельхоз продукции, способствует использованию сульфата аммония в сельском хозяйстве. Известь нейтрализует излишнюю кислотность почвы. Задача. 1 вариант. Сколько килограммов карбоната аммония нужно внести на 100 гектаров, если норма на один гектар составляет 56 кг азота 2 вариант. Сколько килограммов сульфата аммония нужно внести на 100 гектаров, если норма на один гектар составляет 56 кг азота.
Из условия понятно, что на 100 гектаров потребуется внести 5600 кг азота. Известно, что карбонат аммония и сульфат аммония содержат одинаковое количество азота - не более 21% , значит (см. вкладку)
5600 кг азота – 21% Х кг карбонат аммония (или сульфат аммония) – 100%
Х = 5600*100/21 = 560000/21 = 26666,66 (кг) или 26,6 тонн карбоната аммония (сульфата аммония) на 100 гектаров.
Если завод удобрений обслуживает 5 сельхоз предприятий с площадью посевов 2000 га каждое, то производительность завода должна составить 5*2000га*0,26т/га = 2600т/год или 2 600 000 кг в год / 300 рабочих дней = 8 666,66 кг в день. Т.образом, средняя производительность завода по сульфату аммония примерно 10 т/сутки.
Для этой производительности (см. уравнения материального баланса):
Вариант 1. Карбонат аммония
Расход ингредиентов на мощность завода 10 т/сут по карбонату аммония Аммиачной воды 1365,15 кг в день 4,16 руб с НДС /кг 5 686 Углекислого газа 3330,40 кг в день 1 руб с НДС /кг 3 260 Итого расход: 8 946 Приход Карбонат аммония 7271,50 кг в день 4 руб с НДС /кг 29 086 Вывод: если вы используете собственный СО2, произведенный в бродильном отделении спиртового завода, то прибыль составит 20 000 рублей в сутки. Без затрат на производство и транспортных! Для того, чтобы увеличить прибыль необходимо увеличить объемы, поскольку мощность бродильного цеха позволяет это сделать (минимум в 7 раз)!
Вариант 2. Сульфат аммония
Расход ингредиентов на мощность завода 10 т/сут по сульфату аммония Аммиачной воды 1365,15 кг в день 4,16 руб с НДС /кг 5 686 Углекислого газа 3330,40 кг в день 1 руб с НДС /кг 3 260 Гипса 10302,69 кг в день 3,1 руб с НДС /кг 31 936 Камень гипсовый 10302,69 кг в день 0,7 руб с НДС /кг 7 212 Итого расход: 40 882 или 16 157 Приход Сульфат аммония 10302,69 кг в день 4 руб с НДС /кг 41 210 Вывод: затраты на гипс съели всю прибыль!!! Но если вы используете гипсовый камень ГОСТ 1340-82, то прибыль составит примерно 21000 рублей в сутки. Без затрат на производство и транспортных! Про увеличение прибыли при помощи объемов в 7 раз для 3х тысячного завода я сказал выше!!! Химическая мелиорация почв Многие почвы в России кислые. Ионы водорода H+, когда они находятся в избытке, вредны для растений. В кислых почвах снижается жизнедеятельность полезных микроорганизмов и бактерий. Физические свойства кислых почв неудовлетворительны – они плохо проницаемы для воздуха и воды. Почвы считаются сильнокислыми, если почвенный раствор содержит ионы водорода в концентрации, не менее чем в 300 раз превышающей их концентрацию в чистой воде. Кислые почвы улучшают посредством известкования, т.е. внесением достаточных количеств известковых материалов. В результате снижения кислотности изменяется и структура почвы: почвы разрыхляются и становятся более проницаемыми для воды и воздуха, так как предотвращается слипание глинистых частиц. На практике для снижения кислотности кислой почвы вместо гидроксида кальция CaOH2 применяют кальция карбонат CaCO3 (известку). Карбонат кальция реагирует с водородними ионами, образуя растворимую соль и оксид углерода: СаСО3 + 2Н+
= Са2+ + Н2О + СО2 Даже действие однократного известкования может сказываться на урожае в течение нескольких лет. Удобрения, которые при относительной влажности воздуха выше
80%, не поглощают влагу, считаются негигроскопичными. Сульфат аммония – пример
негигроскопичного удобрения.
Вариант 3. Сульфат-нитрат аммония
По 2 варианту мы получили сплав сульфата аммония с известняком в соотношении 60 : 40. Если почва сельхоз предприятия достаточно заизвесткована, то имея достаточное количество аммиачной селитры NН4NО3 можно получить и наиболее удобно применять сплав нитрата аммония (аммиачная селитра - NН4NО3) с известняком (СаСО3), называемый известково-аммиачной селитрой. За границей ее используют довольно широко, особенно в странах Западной Европы. Этот продукт выпускают в виде гранул с различными весовыми соотношениями NН4NО3 : СаСО3 – от 80:20 до 53:47.
Наилучшие физические свойства имеет известково-аммиачной селитра, содержащая 60% NН4NО3 и 40% СаСО3 при этом соотношении компонентов конечный продукт содержит 20.5% N (т.е. 20,5% азота). При смешении известняка с плавом нитрата аммония появляется небольшое количество нитрата кальция Са(NО3)2 (0.4-1.2%). Поэтому продукт более гигроскопичен, чем чистая аммиачная селитра NН4NО3+ СаСО3 = (NН4)2СО3 + Са(NО3)2.
Так как карбонат аммония разлагается уже при 58 градусах Цельсия (NН4)2СО3 =2 NН3 +СО2 +Н2О,
то в плаве, имеющем значительно более высокую температуру, карбоната аммония (NН4)2СО3 не остается. Вследствие этого потери азота в виде аммиака составляют 0.3-0.8 от содержания азота в плаве. Из-за дополнительных затрат (стоимость известняка, расходы на его размол) стоимость азота в известково-аммиачной селитре на 10-15% выше, чем в аммиачной селитре.
Значительная гигроскопичность и слеживаемость нитата аммония затрудняют его хранение и применение в странах с теплым и влажным климатом. Сплавлением с другими солями, с которыми нитрат аммония вступает в химические взаимодействия, например, с сульфатом аммония или хлоридом калия, могут быть получены менее гигроскопичные удобрения с лучшими физическими свойствами
NН4NО3 + (NН4)2SО4 = (NН4)2SО4*2 NН4NО3 нитрат аммония сульфат аммония сульфат-нитрат аммония
Сплав
нитрата аммония и сульфата аммония – это сульфат-нитрат аммония выпускают
за границей в небольших количествах.
|
|||||||||||||||||||||||||||||||||||||||||||||||||
Назад, на главную страницу