|
||||||||||
|
Ферментация
Производители ферментных препаратов для спиртовой промышленности
Ферменты Ново Нордиск для спиртовой промышленности
Производство, получение и культивирование микробных ферментных препаратов для спиртовой промышленности ->
Тепловые схемы ректификационных установок с цехом упаривания барды
Технология кормовых дрожжей на послеспиртовой барде
Анаэробная очистка барды на биологических очистных сооружениях с последующей аэробной доочисткой
Производство кормового концентрата витамина В12 и метана метановым брожением послеспиртовой барды
Получение сбалансированного белково-углеводного кормопродукта (БУК).
Центрифуга для обезвоживания послеспиртовой барды
Общие сведения о брагоперегонных и дистиляционных аппаратах
Расчет дефлегматоров и холодильников брагоперегонных аппаратов
Замена кожухотрубного дефлегматора на пластинчатый
Руководство по проектированию и диагностированию теплообменников для конденсации
Сложная перегонка бражки в спирт
Материальный баланс бражной колонны
|
Производство, получение и культивирование микробных ферментных препаратов для спиртовой промышленности.
Производимые и используемые импортные ферментные препараты для спиртовой промышленности стоят ~ 20 Евро за 1 килограм. Значит, собственное производство ферментов значительно снизит затраты на производство спирта. Из производственного расчета продуктов для выработке спирта из крахмалистого сырья с заменой солода для осахаривания сусла ферментами глубинных культур известно
Например, расход импортных ферментов для осахаривания составляет 2 литра на 100 дал спирта
Цена 1 литра импортных ферментных препаратов для спиртоаой промышленности - 20 Евро
Расход импортных ферментов для спиртового завода мощностью 3000 дал спирта в сутки составит 60 литров/сут. или 60 л х 330 суток = 19 800 литров/год. Издержки на приобретение импортных ферментов для спиртзавода мощностью 3000 дал/ сут составят 19 800 литров/ год х 20 Евро = 396 000 Евро/ год
Расход импортных ферментов для спиртового завода мощностью 15 000 дал спирта / сутки составит 300 литров в день или 300 л х 330 дн = 99 000 литров / год. Издержки на приобретение импортных ферментов для спиртзавода мощностью 15 000 дал/ сут составят 99 000 литров в год х 20 Евро = 1 980 000 Евро в год
Производство, получение и культивирование микробных ферментных препаратов для спиртовой промышленности возможно благодаря разнообразным микроорганизмам. В зависимости от состава питательной среды и условий производства и культивирования микроорганизмы продуцентов ферментов легко переключаются с синтеза одного фермента на другой. У микроорганизмов сравнительно короткий цикл развития (10—100 часов), что позволяет получать сотни урожаев в год. Продуцентами ферментов могут быть:
Для промышленного производства и получения ферментных препаратов используются как природные штаммы микроорганизмов, выделенные из естественных сред, так и мутантные, генно-модифицированные, т.е. селекционированные воздействием на природные микроорганизмы физических и химических мутагенов. Микроорганизмы синтезируют одновременно комплекс ферментов, но некоторые из них, особенно мутантные штаммы, продуцируют в значительных количествах лишь один фермент. Для лучшего использования крахмалсодержащего сырья в спиртовом производстве осахаривающие материалы должны содержать не только амилолитические ферменты, но и ферменты, гидролизующие другие углеводы сырья — целлюлозу и гемицеллюлозы. Для обеспечения дрожжей азотистым питанием имеют значение и протеолитические ферментные препараты. Несмотря на то, что для успешного осахаривания зернового затора нужен комплекс ферментов, отбор микроорганизмов-продуцентов до сих пор проводился главным образом по высокой активности амилолитических ферментов — a-амилазы, глюкоамилазы и в более ранних работах — олиго-1,6-глюкозидазы (декстриназы). Наиболее часто в
качестве продуцентов амилолитических ферментов в спиртовом производстве используются: Для получения амилаз широко применяют
плесневые грибы рода Aspergillius, видов niger, orizae, usamii awamori, batatae; рода Rhizopus, видов delemar, tonkinensis, niveus, japonicum и др., а также отдельные представители Neurospora crassa и Mucor. Плесневые грибы очень
широко распространены в природе; основное место их обитания — почва. Несмотря
на наличие многих родов и видов плесневых грибов все они характеризуются
нитевидным строением тела и специфическим строением плодоносящих органов. Тело гриба состоит
из длинных переплетенных нитей сероватого или белого цвета, называемых гифами. Гифы
распространяются по поверхности питательного субстрата, образуя мицелий и
частично врастают в него. Некоторые гифы, поднимающиеся над поверхностью в виде легкого пушка, имеют
более сложное строение и представляют собой органы плодоношения, называемые
конидие или спорангиеносцами. У мукоровых грибов на конце спорангиеносца находится
шаровидное вздутие, окруженное оболочкой, внутри которого образуются споры. У
аспергиллов конец конидиеносца имеет булавовидное утолщение, от которого
отходят удлиненные клетки, называемые стеригмами; от стеригм отшнуровываются
более мелкие круглые клетки — конидии. Отделившиеся конидии
или споры, попадая в благоприятные условия, начинают прорастать, затем гифы
ветвятся, образуя мицелий; при истощении питательных веществ в среде гриб
переходит - в стадию споро- или конидиебразования. Споры и конидии плесневых грибов
содержат пигменты, что и придает зрелым культурам характерную окраску. На рис. 1 показана морфология
плесневых грибов. Для осахаривания на спиртовых заводах чаще используются
аспергиллы: при поверхностном культивировании — Asp. oryzae и Asp. awamori, а в последнее время высокоактивный по
глюкоамилазе штамм Rhizopus delemar В; при глубинном
культивировании — Asp. niger, Asp. usamii, Asp. awamori и Asp. Batatae.
Рисунок 1. Плесневелые грибы: 1 – Asp. Oryzae; 2 - Asp. Niger, 3 – Penicillium, 4 – Mucor, a – мицелий; б – конидиеносцы в - конидии и споры
На спиртовых заводах США используется высокоактивный штамм Asp. awamori МКК-3112. Аспергиллы являются типичными аэрофилами, поэтому они могут развиваться только на поверхности твердой или жидкой среды или в жидкой, достаточно аэрируемой среде. Оптимальная температура для, большинства аспергиллов 25—30°С, для некоторых — до 35°С. Большинство грибов при поверхностном культивировании могут переносить кратковременное повышение температуры до 40 и даже 45°С без заметной потери активности ферментов. Оптимальная влажность среды для них около 65%. Для питания аспергиллов необходимы азотистые и минеральные вещества. В качестве источника углевода кроме моносахаридов, многих олиго- и полисахаридов могут служить спирты и органические кислоты, однако для накопления амилазы в среде обязательно должны присутствовать крахмал, декстрины или мальтоза. На средах, содержащих другие сахара, в том числе глюкозу грибы амилазы не образуют. Источником азота могут быть белки и их гидролизаты, аммонийные соли и нитраты. Среда должна содержать соединения, в состав которых входят сера, фосфор, калий, магний и микроэлементы. Большинство плесневых грибов усваивают серу из сульфатов, а фосфор — из солей фосфорной кислоты. Аспергиллы не нуждаются в готовых витаминах и факторах роста, так как способны сами синтезировать их из более простых химических соединений, содержащихся в среде. Препараты ферментов из плесневых грибов содержат, как правило, широкий набор ферментов, поэтому во многих случаях могут полностью заменять зерновой солод. В последнее время на спиртовых заводах стал широко применяться высокоактивный по глюкоамилазе штамм Asp.awamori-466, выращиваемый на концентрированном кукурузном сусле 18% сухих веществ). Готовая культура имеет активность до 250 ед. ГлА на 1 мл, но других амилолитических ферментов, а также протеазы практически не образует. В связи с этим эту культуру целесообразно применять в смеси с другими культурами, продуцирующими a-амилазу и протеолитические ферменты.
Дрожжеподобные организмы как продуценты ферментовАмилолитические ферменты синтезируют также некоторые дрожжи и дрожжеподобные грибы родов Saccharomyces, Candida, Endomycopsis и Endomyces. В спиртовом производстве нашли применение End. bispora и End. species 20-9, выращиваемые глубинным способом и продуцирующие главным образом активную глюкоамилазу; а-амилазная активность проявляется слабо. Высокоактивный штамм End. bispora имеет разветвленный мицелий, образует бластоспоры; гифы — септированные, зернистые. На твердых агаризованных средах образует колонии с воздушным серовато-белым мицелием, на жидких питательных средах — гифы и некоторое количество бластоспор. Дрожжеподобные грибы в спиртовом производстве самостоятельно не применяются, так как не содержат других ферментов, необходимых для нормального осахаривания сусла из крахмалсодержащего сырья. Обычно они используются в смеси с ферментными препаратами из плесневых грибов или бактерий.
Бактерии как продуценты ферментовМногие бактерии,
способны синтезировать активные амилазы: Bac. subtilis, Bac. diastaticus, Bac. mesentericus, Bac. mecerans, Вас. polymyxa и некоторые другие.
Бактерии , как продуценты амилолитических ферментов, представляют собой палочки длиной 1,2—1,3 мкм и диаметром 0,6—0,8 мкм. Палочки соединяются по две, три, иногда образуют цепочки. Цикл развития у бактерий короче, чем у плесневых и дрожжеподобных грибов. Например, культура Вас. diastaticus выращивается в глубинных условиях при температуре 60 °С в течение 10—12 часов Бактерия Вас. mesentericus ПБ-ВНИИПрБ, применяемая в на стоящее время на спиртовых заводах как продуцент а-амилазы в смеси с препаратами глюкоамилазы, выращивается в течение 24—36 часов при температуре 40 °С. Особенность бактерий
— их способность образовывать высокоактивную термостойкую а-амилазу, необходимую
на стадии подваривания замесов и осахаривания сусла для разжижения и декстринизации крахмального клейстера. Ферменты микробного происхождения применяются в спиртовом производстве в виде естественной культуры — сухой поверхностной или жидкой глубинной, а также в виде концентрированных препаратов. При определении названия ферментного препарата учитывают только основной фермент, активность которого в препарате превалирует. Название каждого препарата образуется из сокращенного названия этого фермента, вида микроорганизма-продуцента и оканчивается во всех случаях на «ин». Например, если продуцентом глюкоамилазы является Asp. batatae или Asp. awamori, то препарат называется соответственно глюкобататин или глюкаваморин; если продуцент а-амилазы — Asp. orizae или Вас. diastaticus, то препарат называется, амилоризин или амилодиастатин. Для препарата, полученного глубинным культивированием, после названия ставится буква «Г», при поверхностном — «П». Условно количество фермента в стандартной глубинной или поверхностной культурах обозначается буквой «х». При этом под «стандартной культурой» понимается готовая культура продуцента, обладающая
строго определенной активностью на единицу массы. Так, глубинную культуру End. biospora называют глюкоэндомикопсин Гх, а поверхностную культуру Asp. oryzae — амилоризин Пх. Цифры перед буквой «х» в наименовании препарата показывают степень очистки фермента: Пх и Гх — это стандартная исходная культура продуцента без какой-либо очистки; П2х и Г2х — жидкий концентрат растворимых веществ исходной культуры, освобожденный от нерастворимой фазы, с содержанием сухих веществ 40 — 50 %; ПЗх и ГЗх — сухие ферментные препараты, полученные высушиванием экстракта из поверхностной культуры или фильтрата культуральной жидкости при глубинном культивировании; П10х и Г10х — сухие препараты, полученные осаждением ферментов из водных растворов органическими растворителями или высаливанием; П15х л Г15х — препараты ферментов, очищенных различными методами; П25х и Г25х — высокоочищенные, но не кристаллические ферментные препараты, содержащие до 20-25 % балластных веществ. Применение высокоочищенных препаратов от 10х до 25х в спиртовой промышленности нецелесообразно, так как они слишком дороги. Для осахаривания разваренной массы пользуются естественной культурой Гх или Пх или практически неочищенными концентрированными жидкими или сухими препаратами П2х, Г2х, ПЗх и ГЗх В табл. 26 приведена характеристика ферментативной активности некоторых препаратов микробных ферментов, применяемых в спиртовой промышленности в России и за рубежом. Препараты глюкаваморин Пх, глюкобататин Гх и амилоризин Пх содержат полный набор ферментов, необходимых для осахаривания. Преимущественно а-амилазной активностью обладают амилодиастатин Гх, амилосубтилин ГЗх и препараты Novo-I и тенназа. Глубинная культура Asp. awamori 466, выращиваемая на концентрированном кукурузном заторе с высотой глюкоамилазной активностью (250 ед. ГлА на 1 мл) и не имеющая других
амилолитических ферментов, может применяться в смеси с солодом либо с бактериальной культурой Вас. mesentericus или Вас. diastaticus. Существует два
способа производства микроорганизмов продуцентов ферментов: Поверхностный способ, применяемый для культивирования плесневых грибов продуцентов ферментов, характеризуется развитием мицелия гриба на поверхности твердого или жидкого субстрата. На жидком субстрате образуется пленка мицелия, продуцирующего не только амилолитические ферменты, но и органические кислоты, инактивирующие их, поэтому пользуются твердыми субстратами с развитой поверхностью — пшеничными отрубями, дробиной послеспиртовой барды, картофельной мезгой и др. Максимальная активность ферментов достигается при культивировании плесневелых грибов на пшеничных отрубях. Зрелая культура грибов вследствие обволакивания частиц пшеничных отрубей мицелием имеет вид плотной войлокообразной массы.
Дробина послеспиртовой барды бедна питательными веществами, и активность ферментов в культурах плесневелых грибов, выращенных на её поверхности, в 4—5 раз ниже, чем на отрубях. При поверхностном культивировании плесневелых грибов на пшеничных отрубях последние должны быть увлажнены и стерилизованы. В стерильных условиях готовят посевную культуру гриба, но сам гриб выращивают в нестерильных условиях в кюветах, устанавливаемых в растильных камерах. Тепло, выделяющееся в процессе роста плесневелых грибов, удаляется продуванием через растильную камеру кондиционированного воздуха. Поверхностный способ производства и выращивания плесневых грибов для спиртовой промышленности имеет ряд преимуществ. Так как во время роста гриба пшеничные отруби не перемешиваются, посторонние микроорганизмы не распространяются по всей их массе и вызывают лишь незначительное местное инфицирование, которое, как правило, не влияет на активность производимых ферментов. Это, однако, не исключает необходимости тщательной стерилизации среды и оборудования. Культуру плесневелых грибов, выращенную поверхностным способом на пшеничных отрубях, впоследствии высушивают до содержания влаги 10 — 11 %. В таком виде она может храниться продолжительное время без значительной потери активности. Это позволяет организовать централизованное снабжение спиртовых заводов сухой культурой плесневых грибов, что является одним из преимуществ поверхностного способа выращивания. Недостаток поверхностного способа выращивания плесневелых грибов — необходимость установки множества кювет, работу с которыми трудно механизировать. Себестоимость культуры гриба-продуцента фермента высока, причем в основном из-за затраты большого количества ручного труда. Механизация процесса выращивания возможна путем создания непрерывно действующих установок или бескюветных аппаратов с вертикальным толстым слоем питательной среды и интенсивным продуванием воздуха через этот слой. Глубинную культуру микроорганизмов
выращивают на жидкой питательной среде при энергичной аэрации стерильным воздухом в герметически закрытых аппаратах и в стерильных условиях. Этот процесс полностью механизирован. Стерильность глубинной культуры микроорганизма — продуцента ферментов для спиртовой отрасли - положительно отражается на
результатах сбраживания разваренного крахмального сусла дрожжами. При поверхностном культивировании твердой
средой обычно служат пшеничные отруби, содержащие в достаточных количествах все вещества, необходимые для питания гриба. Лучшие результаты достигаются при содержании крахмала в отрубях или в другой питательной среде не менее 16 %. С целью удешевления питательной среды А.
А. Шилова и Р. В. Фениксова предложили применять в качестве основы ее биошрот — отход производства ферментов, представляющий собой нерастворимый остаток культуры после экстрагирования ферментов. При обогащении крахмалом и ростовыми веществами, вносимыми соответственно с картофельной мезгой и солодовыми
ростками, получается полноценная питательная среда. Основой может служить также пивная дробина, к которой добавляют разваренную массу зерно-картофельного сырья. На некоторых спиртовых заводах используют питательную среду,
составленную из 80 % картофельной мезги (крахмалистостью 15—16% и влажностью 70—74%), 17% пшеничных отрубей и 3% сухих ростков
ячменного солода (отхода пивоваренного производства). В Чехословакии применяют смесь, состоящую
из 30% картофельной мезги, 30% дробленой подсолнечной лузги, 30% стержней кукурузных початков и 10% отрубей, к которой добавляют 6% кукурузного экстракта или сгущенного клеточного сока картофеля. Получение посевного материала для производства плесневелых грибов продуцентов ферментов в спиртовой промышленности Для засева производственной питательной среды может быть использован посевной материал трех видов: Споровой материал готовят поверхностным культивированием плесневелого гриба на твердой или жидкой питательной среде в специальных аппаратах с кюветами. В первом случае гриб выращивают в пробирке на косом агаре до обильного образования спор, затем спорами засевают колбы со стерильными пшеничными отрубями, наконец, спороносящую культуру передают в специальный аппарат. По окончании спорообразования в этом аппарате отбирают споры посредством специального вибросепаратора при тщательной аспирации. Споры гриба фасуют в полиэтиленовые мешочки, стеклянные или дюралюминиевые банки, в которых они могут сохраняться при температуре от 8 до 24 °С около 1,5 лет. Во втором случае из спор, собранных в пробирке с косым агаром, готовят водную суспензию и ею засевают жидкую питательную среду, которую направляют в растильный аппарат. Из-под выросшей спороносящей пленки удаляют жидкую среду, пленку подсушивают, снимают с кювет, измельчают и упаковывают. Готовый споровый материал не содержит примеси среды и обладает высокой всхожестью (90—95%), которая сохраняется свыше 3 лет. Споры гриба (конидии), полученные любым методом, обладают водоотталкивающей способностью и почти не смачиваются водой. Это их свойство приводит к неравномерности засева среды и, следовательно, к неодинаковой скорости роста культуры. Смачиваемость спор можно улучшить, если добавить в их водную суспензию 25 — 50 мг поверхностно-активного вещества, например алкилбензол-сульфата, на 1 г спорового материала. При этом всхожесть спор остается без изменения. Для сокращения длительности культивирования плесневых грибов в производственных условиях можно применять предварительное проращивание спор в течение 7 часов в жидкой питательной среде До появления ростовых трубочек. Это сокращает продолжительность лаг-фазы на 8 — 9 часов и увеличивает оборачиваемость растильных камер. Применение спорового материала упрощает технологический процесс, позволяет более полно механизировать его и сократить площадь цеха чистой культуры. Централизованное производство спорового материала для группы спиртовых заводов, работающих с данным штаммом гриба, выгодно создать в одном специализированном Цехе Чистой Культуры. Положительный опыт подобной организации имеется в производстве лимонной кислоты методом микробного синтеза. Л.С. Салмановой предложено засевать производственную питательную среду мицелием, полученным глубинным культивированием гриба в 10-литровых колбах на качалке. При высокой производительности предприятия целесообразно выращивать посевной мицелий в небольших ферментаторах, как это было предложено А. П. Левчиком и осуществлялось на Мичуринском экспериментальном ферментно-спиртовом заводе в Тамбовской области. Получение в глубинных условиях неспороносящего посевного мицелия значительно улучшает санитарные условия труда, сокращает производственные площади и способствует росту производительности ферментного цеха. На спиртовых заводах получило распространение приготовление посевного материала в виде поверхностной культуры плесневелово гриба на пшеничных отрубях, которое складывается из следующих двух операций: 1) выращивание спороносной культуры гриба в пробирках на сусло-агаре; 2) засев спорами пшеничных отрубей в колбах и выращивание культуры гриба. Культуру получают из лаборатории чистых культур ВНИИПрБ. Исходная — музейная чистая культура хранится в холодильнике при температуре от 2 до 4 °С. Один раз в месяц пересевают споры музейной культуры из пробирки в пробирку с сусло-агаром с соблюдением правил проведения микробиологических работ. При этом первая засеянная пробирка является музейной, а остальные 2 — 3 пробирки используются для дальнейшего размножения. Засеянные пробирки помещают в термостат при температуре 30 °С и выдерживают в нем в течение 4—6 суток. При нормальном росте
поверхность сусло-агара равномерно покрывается спороносящим мицелием. Культура плесневелого
гриба с плохим спороношением, с медленно растущим мицелием, с пушком вторичного роста в
производство ферментов не допускается. Пробирки с выросшей культурой вынимают из термостата и
хранят в холодильнике. Перед посевом в колбы проверяют чистоту культуры высевом на
чашки Петри и микроскопированием. Чистая культура на
сусло-агаре служит исходным материалом для размножения плесневелых грибов на пшеничных отрубях в
колбах. Отруби смешивают с водопроводной водой в соотношении 1 : 0,7 и переносят в несколько колб
по 10—20 грамм в каждую. Колбы закрывают ватными пробками и стерилизуют в автоклаве при
избыточном давлении 0,15 МПа в течение 1 ч. После охлаждения до комнатной температуры в колбы
вносят суспензию спор гриба, содержащую 150— 200 тыс. спор в 1 мл. Для этого в пробирку с культурой
гриба на сусло-агаре прибавляют 10 мл стерильной водопроводной воды и при
помощи стерильной пипетки над огнем соскабливают конидии гриба. Полученная
суспензия используется для посева (2—2,5% от массы засеваемой среды или 0,4—0,5
мл на 10 грамм отрубей). Выращивание ведут в
термостате при температуре 30 °С в течение 4—5 суток. Одну из колб используют для
дальнейшего размножения чистой культуры, остальные хранят в холодильнике для последующего цикла. В
колбу, предназначенную для размножения, вливают 50—60 мл стерильной водопроводной
воды и над пламенем стерильной пипеткой тщательно перемешивают. Расход чистой
культуры при пересеве из колбы в колбу или банку составляет 5—10% от массы
засеваемой среды. Размножение посевного материала для производства плесневелых грибов как продуцентов ферментов для спиртовой промышленности Пшеничные отруби для выращивания на них посевного материала плесневелых грибов подготавливают так же, как и при получении чистой культуры.
Отруби, стерилизованные в бюксах под избыточным давлением 0,15 МПа в течение 1,5 часов, переносят на специальный стол, предварительно вымытый и дезинфицированный. Охлаждение отрубей до температуры 40—42°С проводят перемешиванием с соблюдением правил микробиологической чистоты. Затем их засевают спорами из колбы с чистой культурой (расход культуры — 0,5—1% от массы отрубей). Суспензию спор готовят из расчета 1 часть культуры на 5 частей воды. Засеянные отруби распределяют по кюветам, предварительно стерилизованным при температуре 120°С в течение 2 ч, слоем толщиной 1—1,5 см. Кюветы сверху закрывают крышкой, под которую подкладывают стерильную бумагу; на отверстие по центру крышки накладывают стерилизованную ватную подушку, после чего кюветы помещают в термостат на 18—24 часов при температуре 30—32°С. В дальнейшем кюветы устанавливают на стеллажи, расположенные в самой растильней камере, и ращение ведут при температуре 24—28°С в течение 3— 4 сут. Выросшую культуру затем помещают в комнату подсушки и в воздушно-сухом состоянии передают на хранение в кладовую, температура в которой не должна превышать 8°С. Посевной материал, приготовленный описанным способом, представляет собой
спороносную культуру гриба, содержащую не менее 0,7 млрд. спор в 1 г, из которых
86—90% способны к прорастанию. Посевной материал не должен содержать посторонней микрофлоры. Производственное культивирование плесневелых грибов продуцентов ферментов для спиртовой промышленности На рис. 56 приведена
технологическая схема получения культуры плесневелого гриба продуцента фнрментов в растильных камерах на кюветах. Этот способ связан с затратой большого количества ручного труда, однако пока применяется на спиртовых заводах. Пшеничные отруби ковшовым элеватором 1 подают на автоматические весы 2, отсюда они поступают в загрузочный бункер 3, а из него в стерилизатор 5. В этом аппарате отруби увлажняются водой, подаваемой через форсунки из бака для стерильной воды 4. На 1 кг отрубей добавляют 0,2 л воды и 7—8 мл соляной кислоты с относительной плотностью 1,19 или 2,7—3,0 мл серной кислоты плотностью 1,84. Стерилизацию производят острым паром при температуре 103—105 °С (давление 0,07 МПа) в течение 1 — 1,5 часов, периодически включая мешалку. По окончании стерилизации отруби дополнительно увлажняют до содержания влаги 58—60 %, охлаждают до 40—42 °С и затем производят засев культурой гриба, полученной в отделении чистых культур. Расход посевного
подсушенного материала составляет 0,5 — 0,6% к массе пшеничных отрубей. Посевной материал
вводится в виде водной суспензии, приготовляемой из культуры гриба в
5-10 кратном количестве кипяченой воды. Засеянную среду
тщательно перемешивают в течение 15- 20 минут, выгружают на раскладочный стол 6
и распределяют по кюветам. Наполненные кюветы ставят в этажерки 7, перевозят их
на тележках в растительную камеру 8, в которой поддерживают ра партии, активности
ферментов и массы. Хранят культуру в сухом помещении на деревянных стеллажах. Предложены технологические схемы производства поверхностных культур плесневых грибов с использованием механизированных растильных установок: с вертикальными каналами (установка была осуществлена на Мичуринском заводе и может быть использована на предприятиях средней мощности — до 2 тонн культуры гриба в сутки); непрерывно действующей конвейерно-пластинчатой, предназначенной для специализированных ферментных предприятий мощностью более 2 тонн культуры в сутки На рис. 57 приведена технологическая схема производства поверхностной культуры плесневых грибов продуцентов ферментов с использованием растильных камер конструкции А. В. Соловьева. Взвешенные отруби загружают в бункер, из которого дозатором передают в шнек-стерилизатор. Стерилизованная среда поступает в выдерживатель, а из него в аппарат для расхолаживания, увлажнения и засева культурой гриба в виде суспензии. Конечная влажность засеянных отрубей около 60%. Расход посевной культуры — 0,5% к массе воздушно-сухих отрубей. Подготовленная и засеянная среда механически загружается в одну из камер для выращивания плесневых грибов в вертикальном слое. Для равномерного распределения отрубей над камерой установлена лопастная мешалка, имеющая частоту вращения около 13 об/мин. Мешалка может перемещаться вдоль камеры и в вертикальном направлении. Уплотнение среды создается с помощью вибратора. Основные технологические операции выполняются на двух ветвях поточной линии: на первой — загрузка и ращение по стадиям, на второй — выгрузка, мойка и стерилизация растильной камеры. Растильные камеры передвигаются на поточных линиях по рельсам. На первой ветви передвижение осуществляется с помощью толкателя, на второй — вручную. Для.перевода растильной камеры с первой ветви на вторую и обратно предусмотрены траверсные тележки, Растильная камера вмещает 500 кг отрубей в расчете на воздушно-сухие. Количество камер 7, из них 6 всегда загружены, а 1 находится на разгрузке, мойке, стерилизации или загрузке. Растильная камера представляет собой ящик прямоугольной формы размером 1600x1300x1620 мм, изготовленный из алюминиевого сплава. Внутри нее имеется 23 вертикальных канала с перфорированными стенками для выращивания гриба; диаметр отверстий 3 мм, шаг 40 мм. Сверху каналы открыты, а снизу закрыты затворами, открывающимися при разгрузке системой рычагов. Щели между каналами шириной 12 мм предназначены для аэрации растущей культуры и отвода выделяемого ею тепла. Кондиционированный воздух подводится с торца камеры и отводится с противоположной стороны. Загруженная растильная камера механическим толкателем продвигается к воздушным диффузорам, которые автоматически с достаточной герметизацией подключаются к растильным камерам. Герметичность создается пневматически. Наилучшие показатели по активности культуры достигаются при поверхностном выращивании гриба на среде, температура которой 15°С. При подаче охлажденного воздуха с относительной влажностью 98— 100% подсыхания среды не происходит; при снижении влажности воздуха до 67—70% влажность питательной среды изменяется мало. Амилолитическая активность культуры возрастает до 36 часов, а затем снижается. Потери сухих веществ за 36 часов составляют около 25%. Общая продолжительность цикла выращивания культуры с учетом подготовительных и заключительных операций в камере 48 часов. Сырая культура из растильной камеры выгружается в бункер, оборудованный специальным устройством для дробления, к шнеками подается в сушилку. Мойку и стерилизацию растильных камер проводят в камере стерилизаторе, где их обрабатывают водой снизу, сверху и с боков, а затем стерилизуют острым паром при температуре 120 °С. После этого подготовленные растильные камеры с помощью траверсной тележки направляют на загрузку. В цехах по производству поверхностной культуры плесневелых грибов продуцентов ферменов во избежание заражения культуры гриба посторонними микроорганизмами соблюдают особую чистоту. Влажную уборку проводят ежесменно, помещение и оборудование периодически дезинфицируют, в цехе работает приточно-вытяжная вентиляция с использованием воздуха, очищенного от микроорганизмов. Готовая культура гриба всегда содержит небольшое количество спор в связи с неодновременным созреванием в отдельных участках, по этому рабочие, непосредственно соприкасающиеся с ней, должны надевать на лицо марлевые повязки, а на руки — резиновые перчатки. Разгрузка кювет и дробление культуры гриба должны проводиться в герметически закрытых камерах, снабженных аспирационными устройствами (вытяжками воздуха).
Глубинное культивирование плесневелых грибов и других микроорганизмов продуцентов ферментов для спиртовой промышленностиПри глубинном культивировании микроорганизмов продуценты ферментов развиваются во всем объеме жидкой питательной среды. Так как большинство продуцентов ферментов — строгие аэробы, то питательную среду интенсивно продувают стерильным воздухом. В микроорганизмах протекают два неразрывно связанных процесса — синтез биомассы и синтез ферментов. Для максимального накопления ферментов необходимы определенный состав питательной среды, обеспечение кислородом воздуха, своевременный отвод метаболитов и физиологического тепла, оптимальные значения рН и температуры. Важнейшим условием является также стерильность питательной среды, подаваемого воздуха, ферментаторов, трубопроводов и арматуры. Питательные среды для глубинного культивирования микроорганизмов - продуцентов ферментов Для глубинного культивирования ферментов в условиях спиртового завода используют жидкие питательные среды, содержащие примесь твердых компонентов. В комплексных питательных средах, основанных на естественном сырье с добавлением отрубей, ростков, кукурузного жмыха, глютена, свекловичного жома, спиртовой барды, следят за тем, чтобы не было крупных комочков, так как они затрудняют стерилизацию и могут привести к забиванию коммуникаций. Поэтому перед смешиванием необходимо проводить просеивание твердых компонентов или грубую фильтрацию (например, зерно-картофельной барды). Жидкую часть питательной среды (вода или фильтрат барды) обогащают питательными солями, гидролизатами белков, аминокислотами, источниками биоса, различными углеводами. Содержание сухих веществ в жидких питательных средах может колебаться от 1,5 до 16% в зависимости от рода продуцента и принятого режима культивирования. Ниже в качестве примера приводится состав питательных сред (в %) для производственного культивирования трех микроорганизмов - продуцентов ферментов.
Питательная среда для Аsp. batatae 61 Грубый фильтрат барды 96,6 Мука кукурузная или пшеничная 1,95 Кукурузный экстракт 0,6 Селитра аммиачная 0,5 Мел 0,2 Магнезит (МgО) 0,1 Растительное масло (пеногаситель) 0,05 Питательная среда для End. biospora Вода 93,75 Кукурузная мука 2,6; Соевая мука 1,5 Кукурузный экстракт 1,6 КН2РО4 или (NН4)2НРО4 0,5 Растительное масло 0,05
Питательная среда для Аsp. awamori 466 - ВНИИПрБ Кукурузный затор, осахаренный ячменным солодом (1,2—3%) 1,2—3 Содержание сухих веществ 18—20 В научно-исследовательских организациях постоянно проводится работа по улучшению эффективности производства ферментных препаратов, в основном по повышению активности зрелой культуры. Это достигается не только селекцией штаммов микроорганизмов, но и совершенствованием условий культивирования, в том числе и изменением состава питательной среды, поэтому приведенные составы питательных сред могут подвергаться значительным изменениям при соответствующем корректировании аэрации и других условий культивирования. Получение и размножение посевного материала Для засева производственной питательной среды при глубинном культивировании посевной материал готовят также глубинным способом. Вид посевного материала зависит от продуцента: для грибов — это мицелиальная масса, для бактерий — молодая растущая культура на начальной стадии спорообразования. Получение посевного материала осуществляется постадийным увеличением массы культуры продуцента. При небольшой производительности цеха она сводится к одной или двум операциям, а для заводов большой производительности представляет собой многостадийный процесс. В качестве примера приводится схема приготовления посевного материала для производственного культивирования двух микроорганизмов. Для Аsp. awamori 466-ВНИИПрБ 1. Пробирка с исходной культурой на агаризованной питательной среде 2. Пересев водной суспензии культуры в колбы с жидкой питательной средой, содержащей 5% кукурузной муки и 0,5% дрожжевого автолизата, культивирование на качалке в течение 48 ч
3. Пересев культуры в сосуды вместимостью 6л (величин f засева 10-12% К объему питательной среды), культивирование 48 часов
4. Пересев культуры в инокулятор на кукурузное сусло концентрацией 6%, культивирование в течение 48 ч при температуре 27°С, перемешивании мешалкой с частотой вращения 950 об/мин и подачей воздуха 16 м3 (мэ-ч) 5. Пересев культуры в производственный ферментатор (величина засева 3% к объему питательной среды)
Для Endomycopsis biospora
1. Пробирка с исходной культурой на агаризованной среде с крахмалом и глюкозой
2. Пересев петлей и получение стационарной культуры на жидкой питательной среде с крахмалом, глюкозой и кукурузным экстрактом в колбах на 100 МЛ (культивирование в течение 48—72 ч в термостате при 28°С) 3. Пересев 4—6% к объему среды в колбах вместимостью 750 мл с 50 мл жидкой питательной среды, включающей крахмал и кукурузный экстракт
4. Пересев 0,3—0,5% к объему среды в маточнике, содержащей крахмал и кукурузный экстракт (культивирование в течение 24 ч при 28°С) 5. Пересев 3—5% к объему среды в производственном ферментаторе. Культивирование на всех стадиях должно проводиться при оптимальной температуре, аэрации и в строго определенное время. Если возникают непредвиденные задержки в использовании, то посевной материал охлаждают до 8—10°С и хранят не дольше 4 ч, иначе качество его может резко ухудшиться. Посевной материал как на отдельных стадиях, так и готовый подвергают тщательному микробиологическому контролю. Посевной материал не должен быть инфицирован посторонней микрофлорой и должен содержать определенное количество спор или клеток на единицу массы, стойко сохранять генетически заложенные в нем свойства продуцировать ферменты.
Производственное культивирование ферментных препаратов для спиртовой промышленностиИзвестны следующие
способы глубинного культивирования плесневелых грибов - продуцентов ферментов: Периодический способ производства ферментных препаратов для спиртовой промышленности характеризуется несменяемостью питательной среды в ферментаторе, состав которой в процессе развития постепенно изменяется. Процесс протекает постадийно: в ферментатор набирают питательную среду и задают посевной материал; после размножения микроорганизмов и накопления продуктов их обмена зрелую культуру выгружают, а все оборудование, коммуникации и запорные устройства промывают и стерилизуют паром. По непрерывно-циклическому способу микроорганизмы, расположенные на неподвижной насадке в ферментаторе, непрерывно омываются средой, протекающей в замкнутом контуре, до полного потребления ими питательных веществ. После этого зрелую культуру выгружают, аппарат промывают, стерилизуют и цикл повторяют. Богатая питательная среда в ходе такой циклической ферментации постепенно истощается; по времени этот процесс более продолжителен, чем непрерывно-проточный. Способ непрерывно-проточного производства микроорганизмов продуцентоа ферментов для спиртовой промышленности более совершенен. Суть его заключается в том, что микробная популяция развивается в проточной питательной среде. Непрерывный способ имеет две разновидности: гомогенно-непрерывный и градиентно-непрерывный. В первом случае выращивание ведут в одном ферментаторе; при тщательном перемешивании среды и аэрации обеспечивается одинаковое состояние культуры во всем объеме жидкости. В ферментатор при этом непрерывно поступает свежая среда, а из него также непрерывно вытекает избыток культуральной жидкости. Градиентно-непрерывное культивирование осуществляют в батарее ферментаторов, соединенных переточными трубами. Засеянная среда с большим содержанием углеводов и других ингредиентов непрерывно перетекает из одного ферментатора в другой и также непрерывно вытекает в виде готовой культуры. Непрерывное культивирование в проточных средах позволяет выращивать микроорганизмы в условиях, оптимальных для их возрастного состояния. При этом такие важные факторы, как концентрация питательных веществ, содержание продуктов обмена, рН, содержание растворенного кислорода, резко изменяющиеся при периодическом способе культивирования, поддерживаются постоянными на заданном уровне или изменяются по усмотрению оператора. Непрерывый способ производства ферментных препаратов для спиртового производства не вышел еще из стадии испытаний. Поэтому в настоящее время на спиртовых заводах применяют периодическое культивирование микроорганизмов.
На рис. 58 приведена технологическая схема установки по получению глубинной культуры фермента для спиртовой промышленности Asp. Batatae 61. Барда из брагоректификационного аппарата поступает в непрерывно действующий фильтр 1 для отделения крупных частиц дробины. Фильтр представляет собой полуцилиндрическое или коническое сито с отверстиями диаметром 1,5—2 мм. С фильтра отбирают 15—20% жидкой части с 0,05% дробины (в исходной барде содержалось ее 1,3 — 2,7%) в сборники 2 и центробежным насосом 3 перекачивают ее в смеситель 9, служащий для приготовления питательной среды. Другие компоненты среды — муку, магнезит и мел — смешивают с водой в сборнике 4, из которого насосом 5 перекачивают также в смеситель 9. В смесителе питательную среду тщательно перемешивают и раствором гидроксида натрия доводят рН до 5,6—5,8. Затем среду стерилизуют, для чего насосом 10 ее подают в контактную головку 8, нагревают с 75—80 °С до 128—130 °С, выдерживают в трубчатом аппарате // в течение 40—50 мин и охлаждают до 30—32 °С в поверхностном теплообменнике 12. Стерилизованная и охлажденная среда поступает в ферментаторы 13 — вертикальные цилиндрические сосуды с лучевыми аэраторами или с двухъярусными турбинными мешалками и барботером для подвода воздуха. В тех случаях, когда теплообменник отключают для профилактического осмотра или ремонта, горячую среду из выдерживателя по обходной коммуникации передают непосредственно в ферментатор. В процессе заполнения ферментатора в нем поддерживают избыточное давление 0,25 МПа паром, подаваемым по воздуховоду через аэрирующее устройство. Коэффициент заполнения ферментатора 0,75—0,85. При меньшем его значении объем доводят до нормы подачей барды из смесителя 9 через систему стерилизации. После заполнения ферментатора всю систему освобождают от среды, прокачивают водой и стерилизуют острым паром. Питательную среду в ферментаторе охлаждают до 30—32°С. В ферментаторе среду засевают культурой плесневелого гриба из маточника 14. До засева из ферментатора отбирают пробы через пробоотборник для микробиологического контроля (высев на МПБ или МПА) и биохимических анализов. Засев осуществляют по линии передавливания, предварительно стерилизованной от маточника до ферментатора острым паром в течение 1 часа. Для этого закрывают вентиль на выходной воздушной линии у маточника и поднимают в нем дабление до 0,06—0,08 МПа, оставляя в ферментаторе давление 0,02—0,03 МПа, после чего открывают вентиль на линии передавливания у маточника и ферментатора и в связи с разностью давления посевную культуру из маточника передавливают в ферментатор. Если маточник один на два ферментатора, то из него передавливают только 50% культуры. После этого закрывают вентили на линии передавливания, в ферментаторе приводят во вращение мешалку и начинают процесс выращивания культуры. Маточник представляет собой цилиндрический сосуд со сферическим днищем, оборудованный устройством для аэрации и перемешивания, патрубками для подачи питательной среды, спуска промывных вод, подачи пара, подвода и отвода воздуха. После передавливания всей посевной культуры из маточника выпускают воздух, открывают крышку и внутреннюю поверхность тщательно моют. Затем маточник стерилизуют и заполняют питательной средой для следующего цикла приготовления посевного материала. Питательную среду для маточника готовят в смесителе 6, оборудованном миксером. Вначале в смеситель набирают воду, включают миксер и постепенно вносят муку, кукурузный экстракт и растительное масло. Размешивание среды производится не только миксером, но и в результате циркуляции ее насосом 7; рН среды доводят серной кислотой до 5,6—5,8. Тем же насосом среду подают через контактную головку 8 в маточник, где ее выдерживают 1,5—2 ч при 126—132СС, охлаждают до 30—32°С и засевают спорами гриба, выращенного в колбах на отрубях, через посевной лючок с соблюдением условий стерильности и при минимальном движением воздуха в цехе. После засева открывают вентили для подачи и отвода воздуха. Расход воздуха 50—60 м3/(м3-ч), его температура 35—40°С. Продолжительность культивирования 36 ч. При задержке передачи посевной культуры в ферментаторы ее расхолаживают в маточнике подачей воды в рубашку и сохраняют при обязательной аэрации. Подготовку воздуха, подаваемого в маточники и ферментаторы, проводят следующим образом. Перед нагнетанием ротационным водокольцевым компрессором 17 воздух очищают от механических примесей на висциновом фильтре 16, а после компрессора освобождают от влаги последовательно в водоотделителе 18, влагоотделителе 19 и конденсаторе 20. Сжатый и осушенный воздух нагревают в теплообменнике 21 до температуры 60—80°С и затем очищают от микрофлоры на общем головном фильтре 22, заполненном базальтовым волокном. После головного фильтра воздух поступает в коллектор 23 и дополнительно очищается на индивидуальных фильтрах 24 у маточника и 25 у ферментатора, которые также заполнены базальтовым волокном. Для бесперебойного воздухоснабжения необходима установка двух головных фильтров. Перезарядку головного фильтра базальтовым волокном проводят 1—2 раза в год, после чего его стерилизуют острым паром при избыточном давлении 0,15 МПа в течение 4—6 часов и затем полностью отдувают влагу горячим воздухом температурой 110—114 °С. Индивидуальные фильтры перезаряжают через 5—10 ферментаций. В случае переброса питательной среды в фильтр или нестерильности ферментации проводят внеочередную перезарядку. Индивидуальные фильтры стерилизуют одновременно с маточниками и ферментаторами острым паром в течение 2 часов при избыточном давлении около 0,2 МПа. Влагу удаляют из фильтров продуванием воздуха. За стерильностью воздуха, поступающего в аппараты, ведут систематический контроль. С этой целью колбу вместимостью 0,5 литров со стерильным мясопептонным бульоном (100—150 мл) в стерильных условиях подсоединяют к специальному пробному кранику на воздуховоде и продувают воздух через бульон в течение 10—12 часов допуская сильного вспенивания). По истечении этого времени колбу отсоединяют и ставят в термостат при 37 °С на 48 часов. Появляющееся помутнение свидетельствует о нестерильности воздуха. Во время глубинного культивирования плесневелого гриба в ферментаторах температура питательной среды 30—32 °С поддерживается автоматическим регулированием подачи воды в рубашку аппарата. Аэрацию воздухом и перемешивание мешалкой (частота вращения около 200 об/мин) проводят непрерывно с момента окончания засева и до конца ферментации. Количество подаваемого воздуха 15—20 м3/(м3-час). Пробоотборник и нижняя сливная коммуникация находятся под паровой защитой. Продолжительность ферментации 48—55 часов. Отработавший воздух из ферментатора по патрубку в крышке выбрасывается через скруббер 26 в атмосферу. В скруббере воздух очищается от спор и других взвешенных частиц. Готовая культура насосом 15 перекачивается в сборники при осахаривателях разваренной массы. Освободившийся ферментатор моют и стерилизуют острым паром при 120 °С в течение 2 часов. В процессе ферментации для микробиологического и биохимического контроля развития культуры отбирают пробы (с соблюдением условий стерильности) вначале через 24 часа после засева, а затем через каждые 12 часов роста. Готовая культура должна иметь активность не менее: по а-амилазе 4—5 ед./мл и по глюкоамилазе — 5—6 ед./мл. Производственное культивирование других микроорганизмов продуцентов ферментов проводится по аналогичной технологической схеме и отличается только составом питательной среды, расходом воздуха, частотой вращения мешалки в ферментаторе, продолжительностью культивирования и активностью готовой культуры. Так, например, для производства ферментного препарата для спиртовой промышленности Asp. awamori 466 используют кукурузное сусло, осахаренное солодом. Разваривают кукурузную муку с водой при мягком режиме. Концентрация сухих веществ в разваренном кукурузном сусле 20%. Стерилизация питательной среды (кукурузного сусла) производится при 125 °С в течение 30—40 мин. Количество посевного материала — 3% к объему питательной среды. Ферментация производится 120—160 часов при 35 °С при работе двухъярусной мешалки с частотой вращения 150—170 об/мин, расход воздуха 20—30 м3 на 1 м3 аэрируемой среды в час, конечный рН 3,5. Активность готовой культуры = 200 — 250 ед. ГлА/мл.
На рис. 59 приведена технологическая схема непрерывного культивирования плесневых грибов на установке, предложенной ВНИИПрБ и испытанной с положительным результатом на Мичуринском спиртовом заводе в Тамбовской области. Установка состоит из батареи ферментаторов, соединенных переточными трубами. Выращенную в маточнике посевную культуру гриба передают в головной ферментатор, в который одновременно поступает готовая питательная среда. По заполнении первого ферментатора культура самотеком поступает во второй, затем в третий и т. д. С помощью лоткового делителя питательную среду можно распределить между первым и вторым головными ферментаторами и таким образом, регулировать развитие культуры, что, кроме того, достигается и скоростью притока. Основная трудность в осуществлении непрерывного культивирования — большая опасность инфицирования, и необходимость частых остановок для проведения профилактической стерилизации.
КОНЦЕНТРИРОВАНИЕ ФЕРМЕНТНЫХ ПРЕПАРАТОВ В СПИРТОВОЙ ПРОМЫШЛЕННОСТИ
Сухая поверхностная культура ферментных препаратов из плесневелых грибов долго сохраняется и выдерживает дальние перевозки. Глубинная культура ферментов плесневелых грибов из-за низкой концентрации в ней ферментов и порчи не может транспортироваться на большие расстояния. Известено лишь несколько случаев, когда Рауденварскпй завод и ООО Восточный (г. Омутнинск, Кировская область) перевозили глубинную культуру End. biospora и Asp. awamori 466 в автоцистернах на 50—70 км для снабжения ею спиртовых заводов. Однако экономически более целесообразно при снабжении других заводов глубинной культурой концентрировать ее. Способы концентрированния ферментных препаратов для спиртовой промвшленности без применения
очистки могут быть различными:
На спиртовых заводах ни один из этих способов не
нашел применения и распространен на специализированных ферментных заводах
Главмикробиопрома. На Мичуринском спиртовом заводе и 1978 г. внедрено концентрирование глубинной культуры ферментных препаратов способом ультрафильтрации, разработанным Н. И. Беловым с сотрудниками. Сущность способа состоит в том, что культуральиую жидкость, содержащую фермент, подают в аппарат под давлением. Жидкость движется по ряду параллельных каналов, образованных полупроницаемыми мембранами. Вода и часть низкомолекулярных веществ проходят через мембраны, а высокомолекулярные вещества, в том числе ферменты, задерживаются и выводятся из аппарата в виде концентрированного раствора (сиропа). На рис. 60 дана принципиальная схема ультрафильтрационной установки
Рис. 60. Принципиальная схема ультрафильтрационной установки для концентрирования ферментных растворов.
УПТ-3, применяемой на Мичуринском заводе для концентрированна ферментов из культуральной жидкости микроорганизмов End. biospora и Asp. batatae 61. УПТ-3 означает: ультрафильтрационная (У) установка с аппаратами на оснопе плоскопараллельных (П)фильтрующих элементов с турбулентным (Т) движением раствора в каналах аппарата, трехступенчатая (3). Установка имеет площадь фильтрации 100 м2 при производительности до 20 м3 по исходной культуральной жидкости. Ультрафильтрации подвергается культуральная жидкость, освобожденная от мицелия и других взвешенных частиц на фильтр-прессе и суперцентрифуге. Культуральная жидкость должна иметь достаточную ферментную активность и не содержать посторонней микрофлоры. Подготовленную культуральную жидкость из сборника 1 насосом 2 подают на установку, состоящую из трех циркуляционных контуров (ступеней)—А, Б и В, в которых поддерживают давление 0,4—0,6 МПа. Каждый контур имеет свой циркуляционный насос 3, регулирующий вентиль 4, расходомер 5, пять ультра-фильтрационных аппаратов 6 (I, II, III, IV, V) расположенных последовательно один за другим, и теплообменник 7. Контуры соединены между собой переточными линиями с регулирующими вентилями 8. Через расходомер контура А культуральная жидкость движется по каналам всех пяти аппаратов и фильтруется. Фильтрат удаляют, а концентрат через регулирующий вентиль переходит в контур Бит. д. В каждом аппарате контура А находится по 35 фильтрующих элементов, а всего их в контуре 175; в аппаратах контура Б по 26 фильтрующих элементов, всего 130; в аппаратах контура В по ф фильтрующих элементов, всего 95. Общее количество фильтрующих элементов в установке 400. Поверхность одного фильтрующего элемента 0,3 м2. Полупроницаемые мембраны фильтрующих элементов изготовляются на основе ацетатов целлюлозы и имеют различный условный диаметр пор, вследствие чего ультрафильтрация может быть использована как для отделения только воды (концентрирование), так и для очистки от балластных веществ. При турбулентном движении жидкости по каналам она разогревается, поэтому в каждом контуре имеется теплообменник для отвода тепла, в котором охлаждающим агентом является холодная вода. Температура жидкости поддерживается автоматически При прохождении культуралыюй жидкости через контур А концентрация ее повышается с 1—2% сухих веществ до 4—5%; в контуре Б —до 8—9% и в контуре В — до 20%. Фильтрат собирают с каждого контура и выбрасывают в канализацию или используют для приготовления замесов в спиртовом цехе. Концентрат с содержанием сухих веществ 20% собирается в отдельном сборнике, откуда идет к потребителям. Потери активности при ультрафильтрации составляют 4—5% от ее величины в исходной осветленной культуральной жидкости. Применение концентрированных препаратов для полной или частичной замены солода ничем не отличается от применения поверхностных или глубинных культур, и может быть использовано одно и то же оборудование.
ПОДГОТОВКА КУЛЬТУР ПЛЕСНЕВЫХ ГРИБОВ
При замене солода глубинной культурой плесневых грибов в ферментатор после окончания ферментации при тщательном перемешивании добавляют 40%-ный раствор формалина из расчета 2 л на 1 м3 культуральной жидкости. После этого культуру перекачивают насосом в расходные чанки, из которых она через дозатор непрерывно поступает в осахариватель. При замене солода сухой поверхностной культурой плесневых грибов или смесью культур их взвешивают, смачивают водой в соотношении 1 : 1 и тщательно измельчают на дробилках, применяемых для дробления солода. Измельченную массу направляют в сборник и смешивают с теплой водой (28—30°С) из расчета 3—4 л на 1 кг исходной культуры. Для стерилизации приливают 20—25 мл 40%-ного раствора формалина на 1 дал суспензии, тщательно перемешивают!5—20 мин, после чего выдерживают в течение 20—30 мин передают в расходные чанки. Если применяют смесь поверхностной культуры плесневых грибов и сырцового солода, например. Asp.awamori или Asp. oryzae и ячменного или ржаного солода, то их дробят вместе и приготовляют водную суспензию также, как солодовое молоко. Расход поверхностной культуры, удовлетворяющей требованиям МРТУ, определяемый по массе крахмала зерна и картофеля, включая крахмал в культуре, составляет 5%, в том числе аваморина П 4% оризина П 1%; при применении смеси солода и поверхностной культуры: на крахмал картофеля и зерна 4% солода и 2% аваморина П или 4% солода и 3% оризина. Расход глубинной культуры микроорганизмов, а также концентрированных препаратов на осахаривание исчисляется из их активности. Ниже приводится пример с культурой Asp. awamori 466. Культура Asp. awamori 466 имеет незначительное количество а-амилазы, поэтому ее необходимо применять в смеси с другими источниками а-амилазы. Например, при полной замене солода глюкаваморином Гх-466 и амиломезентерином Гх-467 расход ферментов рассчитывают, исходя из норм расхода ферментов в единицах активности на 1 г перерабатываемого крахмала сырья. Причем этот расход изменяется в зависимости от принятой продолжительности брожения. Так, при 72-часовом брожении расход а-амилазы должен составлять 1,5 ед. АС на 1 грамм крахмала, глюкоамилазы — 6 ед. на 1 г крахмала. При 48-часовом брожении расход а-амилазы остается неизменным, а глюкоамилазы увеличивается до 15 ед. ГлА на 1 г крахмала. При этом показатели выбраживания получаются не хуже, чем при 72-часовом брожении. Аналогично ведется расчет и с другими препаратами микроорганизмов — источниками а-амилазы. Препарат а-амилазы рекомендуется подавать в две точки технологической схемы: 0,5 ед. АС — на разжижение подвариваемой массы в предразварник и 1 ед. АС на 1 г крахмала — в осахариватель вместе с глюкоамилазой. Если препарат а-амилазы содержит и другие амилолитические ферменты, в частности глюкоамилазу, то следует учитывать их и соответственно сокращать расход глюкоаваморина Гх-466. Так как активность глюкаваморина Гх-466 может быть очень высокой (250 ед./мл), то для лучшего дозирования ее рекомендуется разбавлять водой из расчета 4—8 м3 на 1 м3 препарата. Препарат глюкаваморин Гх-466 можно применять и в смеси с солодом. В этом случае в зависимости от расхода солода рассчитывается и расход препарата в единицах ГлА на 1 г кархмала. Так, при 72-часовом брожении при расходе зерна на солод 5% к массе перерабатываемого крахмала необходимо 4 ед. ГлА на 1 грамм крахмала, а при расходе солода 8% —3 ед. ГлА на 1 г крахмала. При 48-часовом брожении расход препарата — 5 и 4 ед. ГлА на 1 грамм крахмала соответственно.
Получение собственных микробных ферментных препаратов.При получение собственных микробных ферментных препаратов на спиртовом заводе возможно по следующим причинам: 1. Замес на посев культуры ферментов берется из уже имеющейся системы разваривания зернового сырья; 2. Технологическое оборудование для производства ферментов - это всего два небольших реактора из которых один - для амилосубтилина, другой для глюкавоморина + воздуходувка и стерильный фильтр для фильтрации воздуха; 3. Увеличения штата призводственного персонала не потребуется, т.к. имеющиеся в штате технологи и лаборанты вполне могут контролировать процесс ферментации. 4. В зависимости от состава питательной среды и условий культивирования микроорганизмы легко переключаются с синтеза одного фермента на другой. У микроорганизмов сравнительно короткий цикл развития (10—100 часов), что позволяет получать сотни урожаев в год. 5. При стоимости импортных ферментных препаратов до 20 Евро за 1 килограм получается неплохая экономия.
Таким образом, потребление импортных ферментов составляет 2 литра на 100 дал спирта
Цена 1 литра импортных ферментных препаратов около 20 Евро
Для спиртового завода мощностью 3000 дал спирта в сутки расход импортных ферментов составит 60 литров в день или 60 л х 330 дней = 19 800 литров в год. Издержки на приобретение импортных ферментов для спиртзавода мощностью 3000 дал/ сут составят 19 800 литров в год х 20 Евро = 396 000 Евро в год
Для спиртового завода мощностью 15 000 дал спирта в сутки расход импортных ферментов составит 300 литров в день или 300 л х 330 дн = 99 000 литров в год. Издержки на приобретение импортных ферментов для спиртзавода мощностью 15 000 дал/ сут составят 99 000 литров в год х 20 Евро = 1 980 000 Евро в год
Расчет был сделан в 2000 году для ОАО Слободской спирто-водочный завод производительностью 3000 дал/сут
Кузнецова Н.А.1
,
Иванова Л.А.1
, д.т.н., проф.
1Федеральное государственное бюджетное образовательное учреждение высшего
образования «Московский государственный университет пищевых производств»
На сегодняшний день наибольшую значимость среди всех выпускающихся
ферментных препаратов занимают препараты, гидролизующие белковые вещества -
протеазы. Они являются одними из особенно важных промышленных ферментов. Такая
популярность протеолитических ферментов объясняется тем, что они могут
использоваться в самых разнообразных отраслях промышленности, включая медицину и
агробизнес.
Кислые протеиназы могут использоваться в изготовлении хлебобулочных изделий
для уменьшения длительности замеса теста при производстве заварных сортов хлеба .
Обширно применяются протеолитические ферменты для растворения различных
белковых помутнений в производстве светлого и темного пива , в создании вин, и для
ускорения процессов фильтрации.
Протеолитические ферменты используются для смягчения животного мяса и
рыбы, что упрощает и ускоряет обработку полупродуктов, впоследствии повышая их
качество. Опыт практического применения ферментов для обработки мяса
свидетельствует о том, что этот способ обработки эффективен для следующих
целеустановок:
размягчение жесткого мяса и увеличение на этой основе объема выработки
натуральных мясных полуфабрикатов (бифштекс);
улучшение качества соленых мясных продуктов;
выработка мясных паст, эмульсий, гидролизатов, применяемых в качестве белковых
обогатителей пищи и в лечебном питании детей и взрослых.
Одновременно проводятся исследования по применению препаратов
протеолитических ферментов для ускорения созревания мяса после убоя, улучшения
уровня качества различных видов колбасных изделий, консервов.
Вдобавок протеиназы могут использоваться в кожевенной промышленности для
обработки кожи: улучшается качество шкуры, сохраняется толщина. Также протеиназы
применяются при очистке натурального шелка в процессе удаления белка с поверхности
шелковой нити.
Протеолитические препараты довольно широко используются в медицинской
промышленности и медицине. Они применяются для приготовления множества
питательных и диагностических сред, для изготовления некоторых лечебных сывороток и
вакцин. Протеиназы различной степени очистки используются в качестве лекарственных
средств для регулирования процессов свертывания крови.
Но самая большая потребность в протеолитических ферментах связана с их
использованием в составе синтетических моющих средств (СМС).
Мировая история создания ферментных препаратов для производства стирального
порошка насчитывает уже около 40 лет. И большую часть этого времени занимает
получение щелочной протеазы, которая является наиболее востребованной добавкой.
Ферментный препарат Протосубтилин Г20Х - препарат высокой степени очистки.
Производится в виде порошка глубинной культуры Bacillus subtilis. Получается
высушиванием ультраконцентрата культуральной жидкости в распылительной сушилке.
Продуцентом Протосубтилина Г20Х является Bacillus subtilis —
грамположительная, спорообразуюшая аэробная почвенная бактерия. Первоначально
была описана в 1835 Эренбергом как Vibrio subtilis, в 1872 была переименована Коном в
Bacillus subtilis. Название "сенная палочка" вид получил из-за того, что накопительные
культуры этого микроорганизма получали из сенного экстракта.
Это палочковидная бактерия, размер 3,5x0,6 мкм. Споры овальные, не
превышающие размер клетки, расположены центрально. Имеет перитрихиальное
расположение жгутиков, подвижная.
Колонии сухие, мелкоморщинистые, бархатистые, бесцветного или бледно-
розового цвета. Край колонии волнистый. Растет на МПА, МПБ, а также на средах,
содержащих растительные остатки, простых синтетических питательных средах.
Хемоорганогетеротроф, расщепляет крахмал, гликоген. Bacillus subtilis условно патогенна
для человека.
Наряду с применением щелочной протеазы в синтетических порошкообразных
моющих средствах, препарат может быть использован в композиции моющих паст и
жидкостей. Во время замачивания и в течение стирки препарат удаляет с тканей все
белковые загрязнения – кровяные выделения, пот, следы молока , увеличивая моющую
способность порошка. Огромный плюс протеазы в том, что она является нетоксичной.
Таким образом, стоит отметить, что бактериальная щелочная протеаза в настоящее
время пользуется большим спросом , и ее производство на данный момент довольно
актуально.
Список используемой литературы:
1. Грачева И.М., Кривова А.Ю. Технология ферментных препаратов.// М.: Изд-во
«Элевар». – 2000. – 512 с.
2. Гребешова Р.Н. и др.Ферменты и технологии для текстиля , моющих стредств , кожи ,
меха //М.;Изд-во «ИГХТУ» 2009.-17с
3. Stredansky M., Kremnicky L., Sturdik E., Feckova A. Simultaneous production and
purification of Bacillus subtilis protease.// Appl. Biochem. Biotechnol., 2003, V. 38(3), P. 269
– 276.
4. Патент C12N9/56 - Bacillus subtilis или Bacillus licheniformis.
|

 Производство собственного амилолитического ферментного препарата Aspergillus Niger на спиртовой барде
Производство собственного амилолитического ферментного препарата Aspergillus Niger на спиртовой барде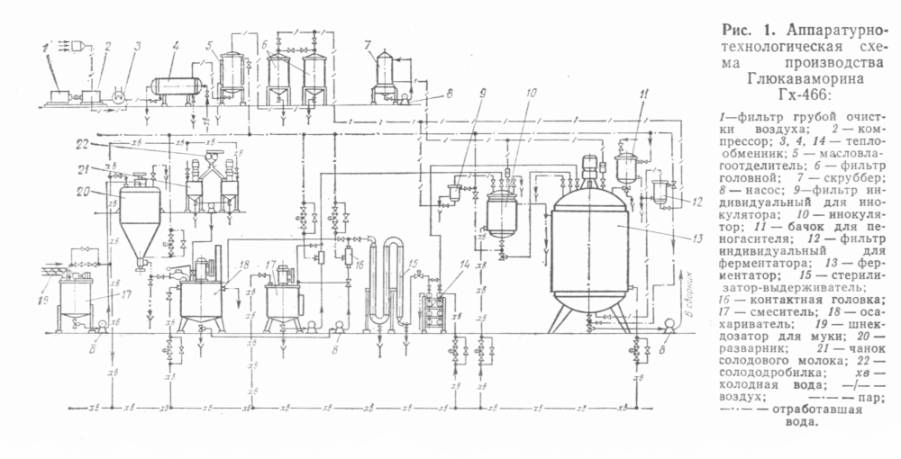 Производство и получение культур микроорганизмов - продуцентов ферментов Глюкавоморин - глубинным способом на послеспиртовой барде спиртового завода
Производство и получение культур микроорганизмов - продуцентов ферментов Глюкавоморин - глубинным способом на послеспиртовой барде спиртового завода Оптимизация производства ферментови и перемешивания культуральной жидкости при непрервыном глубинном культивировании микроорганизмов
Оптимизация производства ферментови и перемешивания культуральной жидкости при непрервыном глубинном культивировании микроорганизмов  Фермент Глюкозоизомераза и её применение в производстве ГФС (глюкозо - фруктозных сиропов)
Фермент Глюкозоизомераза и её применение в производстве ГФС (глюкозо - фруктозных сиропов)






