|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
ПРОИЗВОДСТВО КРАХМАЛА Технологический поток производства крахмала. Структура, свойства, классификация нативных крахмалов. Технологические схемы производства крахмала. Научно-техническая концепция развития производства крахмала. Избирательное разрушение структуры зерна и другого крахмалсодержащего сырья =>
Комплексная переработка зерна пшеницы на предприятиях спиртовой промышленности. Производство крахмала и глютена от компании Альфа-Лаваль. Технология пшеничного крахмала и глютена от ВНИИ крахмалопатоки Методы определения количества и качества клейковины в пшенице. Комплексная переработка зерна ржи на крахмал и спирт Технология кукурузного крахмала Производство крахмалопродуктов из зерна кукурузы на спиртовых заводах Технология картофельного крахмала Отходы кукурузо- и пшенично-крахмального производства Аппаратура для утилизации отходов производства крахмала и получения сухой биомассы Использование экстракта (замочной воды) кукурузы и пшеницы. Выпарные Установки для выпаривания продуктов гидролиза крахмала. Выпарные установки ВУ для сгущения кукурузного экстракта. Сушка продуктов и отходов крахмало-паточного производства.
ПРОИЗВОДНЫЕ ОТ КРАХМАЛА и ИХ ПРИМЕНЕНИЕ
Анализ использования рабочего времени Глюкозо-фруктозные сиропы ГФС взамен сахара и солода в производстве пива Кукурузные сиропы с высоким содержанием фруктозы на рынке альтернативных подслащивающих средств.
Технология высоко-фруктозных сиропов от компании Фогельбуш
Производство глюкозного сиропа и глютена
|
Избирательное разрушение структуры зерна и другого крахмалсодержащего сырья, способы замачивания, разрушения и гомогенизации
Целью избирательного разрушения структуры зерна и корнеклубнеплодов является высвобождение из них целых зерен крахмала, разрыв их связей с другими компонентами сырья без излишнего измельчения твердых веществ, а также получение растворимых веществ в виде концентрированного раствора. Для разрушения структуры зерна и другого крахмал содержащего сырья с целью извлечения крахмала применяются физические, химические и биологические способы воздействия, выбор вида которых обусловлен строением, структурой и технологическими свойствами перерабатываемого сырья. При извлечении крахмала из корнеклубнеплодов, у которых зерна крахмала находятся в клетках и имеют слабую связь с их стенками и растворимыми веществами, ставится задача разорвать эти стенки при минимальном разрушении клеток. Для этих целей применяются ударно-истирающие способы измельчения без предварительного разрушения структуры сырья, например - картофельные тёрки. В зерновом и зернобобовом сырье зерна крахмала также находятся в клетках, но они прочно связаны с твердыми веществами (в основном с белками), поэтому для извлечения крахмала необходимо не только разрушить внешние оболочки зерна и стенки клеток, но и ослабить и разорвать его связи с белками. Решение этой задачи основано на способности белков зерна (альбуминов, глобулинов, глютелинов, проламинов) избирательно растворяться в воде, спирте, слабых щелочах и кислотах. Однако для некоторых видов зернового сырья при химических способах разрыва связей крахмальных зерен с белковыми веществами происходит частичное разрушение клетчатки и гемицеллюлоз с образованием слизей - комплексов некрахмальных полисахаридов (пентозанов) и белковых веществ, что затрудняет отделение от них зерен крахмала. Более эффективен в этом случае биологический метод с использованием протеолитических и целлюлолитических ферментных препаратов (ферментативный гидролиз). Для избирательного разрушения макроструктуры зернового сырья, т.е. для разрыва оболочек и отделения зародыша, широкое применение получил ударный способ измельчения. При определенной скорости удара по замоченному зерну с уже ослабленной структурой пластические деформации не успевают развиться, и оболочка разрушается по образовавшимся микротрещинам и поверхностям раздела эндосперма с зародышем. Отделение частиц эндосперма от семенных оболочек также успешно решается ударным способом [42,38,53]. Прочность связей зерен крахмала с белками и стенками клеток эндосперма неодинакова для различных видов зернового и зернобобового сырья. Так, в сравнении с кукурузой она намного выше у пшеницы, ржи, ячменя, поэтому для разрушения этих связей применяется разновидность ударного способа - кавитационный - с помощью гомогенизаторов видно-мучной суспензии[40,80].
Разрушение структуры зернового сырья при замачивании в водеЗамачивание зерна - это процесс гидро-термической обработки зернового и зернобобового сырья с целью размягчения их роговидной части, разрыва и разрушения белковой цементирующей прослойки, удерживающей крахмальные зерна в клетках эндосперма. Выведение растворимых веществ зерна в замочную воду - это наиболее древний и широко распространенный способ изменения и ослабления структуры зернового сырья. Исследованию процесса замачивания посвящены работы, многих ученых в нашей стране и за рубежом [56,57,76,101]. Их цель - установить основные закономерности физико-химических процессов, происходящих в зерне при замачивании. При этом зерно рассматривалось на молекулярном уровне как комплекс высокополимеров углеводного и белкового происхождения, особенностью структуры которых является отсутствие прочной кристаллической решетки. В связи с этим в глубь высокополимеров могут внедряться адсорбированные молекулы. Это вызывает набухание компонентов сырья, особенно при образовании водородных связей, как это наблюдается при взаимодействии зерна с водой. Из-за беспорядочного расположения активных центров в объеме зерна адсорбированные молекулы воды группируются вокруг активных центров в виде гроздьев, не образуя сплошного, непрерывного мономолекулярного слоя. Однако условно можно представить, что активные центры равномерно распределены на некоторой плоскости поверхности, на которой возможно образование моно- или полимолекулярного слоя. Механизм сорбционного взаимодействия зерна с водой может быть представлен следующим образом. Зерно по массе сухих веществ более чем на 90% состоит из гидрофильных биополимеров — белков и углеводов. Их макромолекулы содержат большое количество функциональных групп, располагающих запасом свободной энергии. Такими группами в углеводах являются —ОН и —О—, а в белках —NH—, —NН2, —СООН, —СОNН2 и т.п. Эти группы атомов выступают в качестве активных центров, непосредственно взаимодействующих с молекулами воды. Иначе говоря, при определенных значениях влажности резко изменяется характер взаимодействия зерна с водой. Несомненно, это должно отражать те изменения свойств зерна, которые обусловлены изменением его влажности. При влажности зерна около 20,5% крахмальные зерна и белковые прослойки между ними в эндосперме имеют одинаковую влажность. В остальных случаях вода в эндосперме распределяется неравномерно: при влажности зерна <20,5% содержание влаги в крахмале выше, чем в белке, при влажности зерна >20,5% - наоборот. При 13—14%-ной влажности белки зерна приобретают повышенную способность к поглощению воды. Это связано с деформацией белковой макромолекулы, раздвижением её боковых ветвей, благодаря чему молекулы воды получают доступ к экранированным ранее активным центрам белковых молекул и заполняют по тину капиллярной конденсации расширившиеся межмолекулярные промежутки. В результате такого неравномерного набухания основных химических компонентов эндосперма в пределах 14-17%-ной влажности физико-химические свойства зерна резко изменяются. Его повышенная гидратация вызывает интенсификацию происходящих в нем биохимических и физиологических процессов. В целом протекающие в зерне при замачивании в воде процессы приводят к изменению его технологических свойств. Внутренний перенос влаги в зерне, механизм распределения ее по химическим веществам и технологические свойства зерна оказываются тесно взаимосвязанными.
Термодинамические особенности взаимодействия зерна с водой. Влагообмен зерна с окружающей средой — это самопроизвольно идущий изотермический процесс; при этом зерно с термодинамической точки зрения представляет собой открытую систему. При его увлажнении происходит диффузионное проникновение молекул воды в его внутреннюю структуру, сопровождающееся изменением энтропии, и адсорбционное связывание молекул воды активными центрами макромолекул белков и углеводов зерна, сопровождающееся тепловым эффектом (изменением энтальпии). Основной причиной процесса может быть любое из этих явлений: необходимо или наличие теплового эффекта, или же возрастание энтропии [57]. При этом самопроизвольный переход молекул из газообразной фазы в адсорбированный слой возможен только при уменьшении изобарно-изотермического потенциала (DG), поскольку наблюдается изобарно-изотермическое сопряжение системы с окружающей средой, т.е.
DG
<
0.
(5.1) Основные термодинамические параметры состояния системы связаны между собой соотношением
DG =
DН - ТDS,
(5.2)
Анализ показывает, что при увлажнении зерна DН <0 и DS < О, но по абсолютному значению | DН | > | ТDS | .
При таком сочетании изменений энтальпии и энтропии обеспечивается
требуемое снижение свободной энергии
DG
, что
и определяет
самопроизвольное развитие процесса поглощения зерном воды. Для оценки процесса связывания воды наиболее показательно изменение энтропии (рис.5.6). Оно имеет отрицательный знак, а по абсолютному значению с повышением влажности (W) убывает, стремясь к нулю в пределах гигроскопического влагосодержания. Снижение энтропии указывает на увеличение порядка структурных элементов зерна на молекулярном уровне, связанное не только с образованием гроздьев сорбированных молекул воды, но и с повышением степени кристалличности, гидратированных белков и углеводов [57] . На графике (рис.5.6) можно отметить два подобных один другому участка: от 0 до 8%-ного содержания влаги и выше 8%. Таким образом, о завершении образования монослоя можно судить по существенному изменению термодинамической характеристики процесса связывания воды. По достижении 15—17% влагосодержания значение энтропии резко снижается. Поглощенная зерном вода переходит в связанное состояние, причем степень этой связи определяется энергетическими уровнями активных центров, а также размерами и структурными особенностями капилляров зерна. Большой практический интерес представляет анализ тех изменений, которые претерпевают свойства связанной воды, поскольку технологические свойства зерна в значительной мере определяются именно энергией связи влаги с его биополимерами, состоянием связанной воды. По классификации академика П. А. Ребиндера, в границах гигроскопического влагосодержания различают химически, физико-химически и механически связанную влагу. Расчет показывает, что основной уровень энергии связи в пределах монослоя составляет 20,9 кДж/моль, т. е. соответствует уровню водородной связи. Это дает основание считать, что в зерне химически связанной влаги нет, поскольку нижний уровень энергии хемосорбции равен 125 кДж/ моль [57]. В зерне в пределах гигроскопического влагосодержания нет и механически связанной влаги, о чем свидетельствует отсутствие в нем макрокапилляров, в которых эта влага может появляться. Наиболее вероятный диаметр капилляров зерна (точнее, размер межмолекулярных промежутков) равен 2,5*10-7 см, следовательно, условий для накопления в зерне заметных количеств механически связанной влаги нет, так как размер макрокапилляров превышает 10-5 см. Таким образом, в равновесном состоянии вся сорбированная в зерне вода связана физико-химически. Однако с повышением температуры и в зависимости от степени завершенности процесса картина может резко измениться. Так, только что прошедшее мойку зерно содержит значительное количество механически связанной воды. Экспериментально установлено и теоретически доказано, что свойства связанной и свободной воды существенно различаются. Наиболее заметна эта разница при анализе термодинамических и некоторых физических ее свойств.
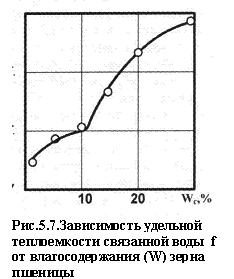
В свободном состоянии вода является одним из наиболее активных растворителей. Адсорбируясь на активных центрах, связываясь ими, она теряет эту способность. Поэтому связанная вода не может активно участвовать в переносе минеральных веществ в объеме зерна. Удельная теплоемкость воды при связывании (г) должна уменьшаться, поскольку этот процесс формально аналогичен фазовому переходу. Значение этого показателя во всей гигроскопической области заметно понижено (рис. 5.7). На графике хорошо выявляется точка, соответствующая завершению образования монослоя и началу интенсивного развития капиллярной конденсации воды в зерне (при W=10%). Степень изменения свойств поглощенной воды связана и с длительностью взаимодействия молекул воды с активными центрами. Каждая сорбированная молекула находится в положении равновесия ограниченный период, продолжительность которого пропорциональна энергии взаимодействия рассматриваемой пары молекула - активный центр. Расчет среднестатистического времени жизни сорбированных зерном молекул воды показывает, что при гигроскопической влажности зерна они находятся во взаимодействии с активными центрами лишь около 10-12 с; затем связь разрывается, молекулы десорбируются, чтобы сразу же локализоваться на другом активном центре или же продиффундировать в окружающую среду; на освободившемся активном центре адсорбируется другая молекула воды. Таким образом, даже в равновесном состоянии при неизменных условиях происходит постоянный влагообмен зерна с окружающей средой, а также внутренняя диффузия влаги по типу "перескоков" молекул воды с одного активного центра на другой. В результате связывания воды все ее свойства претерпевают изменения, степень которых определяется энергией связи. Процесс сопровождается значительным тепловым эффектом, а также изменением плотности воды; следовательно, происходит фазовый переход первого рода - связанная вода отличается от свободной фазовым состоянием. Существенно влияет на свойства связанной воды температура. При ее повышении заметно снижается энергия связи влаги, вода приобретает более высокую подвижность, создаются условия для развития в зерне различных биохимических процессов. То, что в пределах гигроскопического влагосодержания вся вода в зерне связана физико-химически, имеет большое технологическое значение. Невысокая энергия связи обеспечивает быстрое смещение динамического равновесия вслед за изменением внешних условий. Особое значение имеет повышение температуры: при этом происходит «плавление связей» адсорбированных молекул воды, а часть их десорбируется с активных центров, образуя свободную воду. Однако вследствие структурных особенностей зерна извлечь эту воду в окружающую атмосферу трудно; оставаясь в его объеме, свободная (точнее - слабосвязанная) вода влияет на физико-химические свойства биополимеров, вызывает повышение гибкости и подвижности боковых цепей их макромолекул. Наряду с расширением межмолекулярных промежутков должно происходить снижение плотности и твердости зерна, влияющее на характер его деформации [57]. Перенос влаги внутри зерна может происходить в различных направлениях и с разной интенсивностью в зависимости от параметров конкретного процесса. Изучение его особенностей имеет, как уже отмечалось, большое практическое значение, так как с ними связано изменение структуры и технологических свойств зерна.
Химические способы разрушения структуры зернового сырья Замачивание зернового сырья в воде является основным способом воздействия на его структуру, однако этот процесс ограничивается деструкцией только водорастворимых белков, поэтому для полного разрыва связей зерен крахмала с другими компонентами сырья применяются растворы сернистой кислоты и щелочи или их соли, выбор вида которых зависит от состава белков в зерне [42, 56]. Наиболее изучен процесс замачивания зерна кукурузы с применением химических реагентов. Он широко используется в производстве кукурузного крахмала и глюкозо-фруктозных сиропов из него и служит основой его моделирования для других видов сырья. Состояние эндосперма и содержание крахмала в зерне в значительной степени определяют потенциальный выход конечного продукта. Зерно с высоким содержанием крахмала легче замачивается и перерабатывается. Значительная массовая доля белка и роговидного эндосперма затрудняет проведение операций извлечения крахмала. В качестве реагентов при замачивании зерна используются растворы либо едкого натра, либо сернистой кислоты, либо комбинированный реагент, состоящий из серной и сернистой кислот. Эндосперм зерна состоит из белка, крахмала, клетчатки, гемицеллюлоз, пектиновых веществ, пентозанов и др. Их способность к влагопоглощению различна и может усилиться под действием различных факторов. Так, крахмал может вобрать до 44%, белок - до 180 % воды. С повышением температуры воды увлажнение зерна ускоряется вследствие снижения вязкости и увеличения скорости диффузионного переноса [76].
Сернисто-кислотный способ замачивания зернового сырьяНа скорость влагопоглощения при замачивании зерна особенно сильно влияют сернистая кислота и ее соли, причем этот эффект растет с повышением концентрации SO2 в растворе. Так, при замачивании зерна кукурузы в 0,22 %-ном растворе SО2 количество поглощенной им воды за первые 8 часов было почти в 2 раза выше, чем при замачивании в воде. В дальнейшем темп влагопоглощения снижается, и конечная влажность такого зерна бывает лишь на 1 -2 % выше. Ускоряющий влагопоглощение эффект наблюдается только при повышении концентрации SO2 до 0,2- 0,3 % [42,82]. Как установлено, из зерна сортов с большим влагопоглощением выход крахмала выше. Зерно с ободранной оболочкой замачивается быстрее, но конечная влажность его ниже, чем зерна с оболочкой, которая способствует осмотическому удержанию части влаги. При замачивании в растворе SO2 вследствие денатурирующего действия сернистой кислоты проницаемость оболочек и клеток зерна увеличивается, в результате чего поглощение им влаги заканчивается через 12-16 часов. При этом разные части зерна поглощают влагу неравномерно: к концу замачивания влажность зернового зародыша составляет примерно 60%, эндосперма - 38-43%.
С увлажнением изменяется и механическая прочность зерна (рис. 5.8). В начале замачивания она резко падает, а через 12 часов составляет только 25 % от первоначальной. Прочность зерна при замачивании в растворе сернистой кислоты снижается сильнее, чем в водном растворе [42]. Зерно при замачивании и набухании увеличивается в объеме. Однако в замочных чанах это увеличение составляет всего 5-10 % от объема сухого зерна. Объясняется это тем, что скважистость нижних слоев расширенного в процессе замачивания и значительно утратившего прочность зерна в чане при сдавливании и под действием вышележащих слоев снижается, как показывают опыты, почти в 2 раза против скважистости воздушно-сухого зерна [42].
Микробиологические процессы [42,76,101]. В производственных условиях значительную часть времени кукурузное зерно замачивается в воде, содержащей его растворимые вещества. Такая среда наиболее благоприятна для развития многих видов микроорганизмов, продукты жизнедеятельности которых, в свою очередь, существенно влияют на протекание процесса замачивания. В 1г массы початков свежеубранной кукурузы насчитывается от 0,5 до 5 тыс. бактерий и от 7 до 42 тыс. плесневых грибов. В начальный период хранения в зерне преобладает типичный представитель эпифитной микрофлоры Pseud. herbicola — 90 % всех микроорганизмов. Кроме того, в нем находится примерно равное количество дрожжей, плесени и других микроорганизмов. При длительном хранении в благоприятных для зерна условиях при снижении до 70 % их общего количества возрастает доля спорообразующих микроорганизмов. Одним из источников инфицирования является повторно используемая для замачивания кукурузы осветленная глютеновая вода. Перед подачей в чаны она насыщается сернистым газом до концентрации 0,1—0,25 %, что приводит к гибели подавляющего количества микроорганизмов, особенно спор плесневых грибов. Однако небольшие дозировки SО2 оказывают незначительное действие на мезофильные и термофильные бактерии. Условия замачивания зерна оптимальны для немногих видов микроорганизмов. В замочном растворе при относительно высокой температуре, низком рН, наличии сернистого ангидрида могут развиваться в основном термофильные молочнокислые бактерии. Как известно, все бактерии, вызывающие молочнокислое брожение, являются анаэробными, но они могут развиваться и в аэрируемой среде. В качестве питания кроме сахаров они используют азотсодержащие соединения, причем в основном органических форм - белки и аминокислоты. При благоприятных условиях клетка бактерии за 1 час вырабатывает молочную кислоту в количестве, в три раза превышающем ее собственную массу. Какое-то время после начала замачивания зерно продолжает оставаться живым. Однако вместе с водой при увлажнении в него поступают вещества, являющиеся ядом для клеток зародыша и эндосперма. Клетки гибнут, их стенки становятся проницаемыми, и через них в замочную жидкость диффундируют углеводы, белки, минеральные и другие растворимые в воде вещества. Под действием занесенных с зерном и водой микроорганизмов начинают протекать различные биологические процессы, в том числе молочнокислое брожение. Проникший в зерновые клетки сернистый ангидрид изменяет структуру белковой матрицы. Белки сворачиваются в глобулы, и скрепляющая крахмальные зерна протеиновая матрица становится рыхлой, высвобождая их. Продолжается действие некоторых ферментов, находящиеся в зерне, - карбогидраз и протеаз. Поскольку концентрация SО2 в зерне нарастает, микробиологические процессы замедляются, величина рН внутри зерна снижается. Происходит некоторое кислотное модифицирование крахмала, вследствие чего частично теряются его нативные свойства. При продолжении процесса замачивания стенки клеток эндосперма становятся рыхлыми, и при измельчении образуется много мелкой мезги, что затрудняет отделение ее от крахмала. Переходящие в растворимое состояние углеводы и белки зерна накапливаются в замочной воде и служат средой для развития микроорганизмов. В связи с этим при замачивании зерна различных видов применяют химические реагенты, обладающие способностью предотвращать развитие нежелательной микрофлоры, а также оказывать влияние на ряд протекающих при этом биохимических процессов. Например, введение реагентов способствует увеличению выхода экстракта, а также повышению его качества. Основным реагентом, значительно угнетающим развитие молочнокислой микрофлоры, является сернистый ангидрид. При 0,45 %-ной концентрации SО2 в растворе молочнокислое брожение не обнаружено. Однако при оценке такого действия SО2 в растворе необходимо учитывать одно очень существенное обстоятельство. Дело в том, что применяемые в производственной практике методы определения количества SО2 в растворе в большинстве случаев не отражают его истинной массы в свободном состоянии, а учитывают также и значительную часть связанного сернистого ангидрида, бактерицидное действие которого совсем не идентично действию такого же количества SО2 в чистой воде. Этим можно объяснить тот факт, что добавление небольшого количества свежего раствора сернистой кислоты в глютеновую воду вызывает больший бактерицидный эффект, чем значительные количества "старого" раствора SО2. При стационарном замачивании зерна в экстракте образовывалось около 6,3 % молочной кислоты к сухим веществам замочной воды, или около 5% к СВ экстракта. С внедрением противоточного способа замачивания создались более благоприятные условия для развития молочнокислого брожения: содержание молочной кислоты в экстракте увеличилось в 2-3 раза. Молочная кислота накапливается более интенсивно при замачивании лежалого зерна, переход в экстракт растворимых веществ из которого осуществляется значительно быстрее, чем из свежего зерна. Основным проявлением молочнокислого брожения при замачивании зерна является увеличение кислотности экстракта. Однако только 30-45 % его титруемой кислотности приходится на долю молочной кислоты. Некоторая часть кислоты переходит в экстракт из зерна. Кислотность здорового зерна составляет 35-45 см3 0,1 М раствора NaОН на 100 г зерна. При его хранении она может значительно увеличиться за счет ряда органических кислот, в том числе молочной. Ранее считалось, что молочная кислота способствует размягчающему действию сернистой кислоты. В связи с этим при разработке технологического режима замачивания зерна стремились создать наиболее оптимальные условия для молочнокислого брожения. Использовался возврат части жидкого экстракта, содержащего молочнокислые бактерии замочной воды. Однако последующие опыты замачивания кукурузы по ускоренному режиму показали, что размягчающее белковую матрицу действие SО2 достаточно высокое и без развития молочнокислого брожения. Имеются сведения о лучшем уваривании экстракта кукурузы, содержащего большие количества молочной кислоты, в результате перехода части осаждающихся солей в лактаты. В то же время при её значительном накоплении в экстракте активизируется растворение нативных протеинов и ухудшаются условия проведения последующих технологических операций. Следует учитывать также, что при молочнокислом брожении в результате действия гетероферментных бактерий кроме молочной кислоты образуются значительные количества газов и летучих органических веществ, с которыми теряется некоторое количество сухих веществ зерна (около 0,5 %). Таким образом, все микробиологические процессы (кроме молочнокислого брожения), протекающие при замачивании зерна, являются нежелательными. Для их предотвращения применяются высокая температура и сернистый ангидрид как антисептик. Однако использование SО2 в больших концентрациях отрицательно сказывается на проведении процесса замачиваниязерна, а повышение температуры вызывает опасность клейстеризации крахмала. При выбранных концентрациях SО2 и температуре тормозятся все виды микробиологической жизнедеятельности, кроме молочнокислого брожения. При замачивании кукурузного зерна наряду с микробиологическими протекают ферментативные процессы, вызываемые ферментами зерна. В ранние фазы спелости в нем обнаружены значительные количества а- и ß- амилазы, причем активность последней почти в 4 раза выше. При созревании зерна активность амилаз, особенно а-амилазы, несколько снижается. Для разных сортов кукурузы она может варьировать в больших пределах. Наибольшей амилазной активностью обладает щиток зародыша. В зерне обнаружены также фосфорилаза, ß -фруктозидаза, а- и ß -глюкозидаза, липаза, протеиназа и др. Некоторыми исследователями указывается на то, что действие многих ферментов активизируется в присутствии незначительных количеств сульфгидрильных соединений, которые могут образовываться в результате реакции SО2 с растворимыми веществами зерна: однако с увеличением концентрации сернистой кислоты до 0,03 % и более активность ферментов падает, но остается выше или на уровне исходной активности фермента в растворах без SО2. Инактивирующее действие определенных концентраций SО2 вызвано в основном снижением рН. Для а-амилаз оптимум рН 4,5, а для B-амилаз — 5,2, оптимальная температура 50°С. Амилолитические ферменты проявляют активность только в начальной стадии замачивания зерна, расщепляя крахмал. В результате их деятельности образуется около 0,15 % мальтодекстринов к массе зерна кукурузы. Оптимум действия липаз: температура 40 °С и рН 8; при рН 5 активность ферментов составляет только 20 % от максимальной, т.е. действие липаз при замачивании незначительно. Протеолитические ферменты проявляют активность на протяжении всего процесса замачивания, но в начале его она выше, а через 30 ч значительно снижается. В замочной воде количество аминного азота растет быстрее, чем общего, что можно объяснить в некоторой степени протеолизом.
Набухание и растворение белков. Особенностью кукурузного зерна является большое различие в содержании белка в разных его частях. Примерно четвертая часть его находится в зародыше и оболочке, остальная в эндосперме. Белок зерна, являясь в основном резервным, расположен в клетках эндосперма в виде тонких перегородок между крахмальными зернами, которые как бы впрессованы в белковую матрицу. В роговидной части эндосперма белок плотной массой окутывает крахмальные зерна, в мучнистой - белковая масса менее плотна, и зерна крахмала не сдавлены ею. При замачивании зерна кукурузы происходит набухание белков. Под действием температуры могут проходить процессы их термической денатурации. Считают, что умеренная (около 40%) тепловая денатурация не влияет на удерживание крахмальных зерен в зерновой клетке, а значит, и на выход крахмала. Наиболее важной реакцией при замачивании зерна является взаимодействие белковых веществ с сернистой кислотой. В результате его происходит кислотная денатурация белка, коренным образом изменяется структура белковых веществ, что способствует высвобождению крахмальных зерен, делает клеточные структуры проницаемыми для диффузионного перехода растворимых веществ в замочную воду. Сернистая кислота в начале замачивания интенсивно адсорбируется зерном, и концентрация ее в замочной жидкости снижается. Однако через некоторое время (16-20 ч) в результате частичного гидролиза связавших сернистый ангидрид белков концентрация SО2 в растворе возрастает. Замачивание зерна сорго осуществляется теми же методами, что и зерна кукурузы. Главное различие этих зерновых культур заключается в форме и размере их зерен. Зерна наибольших размеров более полно адсорбируют воду, и из них более полно извлекаются растворимые вещества, чем из мелких зерен. Для производства сортового крахмала в основном пригодно оборудование кукурузокрахмальных заводов. Однако форма, размеры, состав и свойства зерен сорго обусловливают и некоторые особенности в конструкции чанов для их замачивания.
Промышленные способы замачивания зернового сырьяОсновными показателями технологического режима замачивания являются температура и длительность процесса, а также концентрация сернистого ангидрида в кислоте (оптимальная - 0,1-0,2%) Общепринятым в последнее время считается температурный предел замачивания 48...50°С. На практике иногда применяют и более низкую температуру, однако это отрицательно сказывается на качестве замачивания зерна. Имеются также рекомендации повышать температуру замачивания до 55 °С при переработке зерна кремнистых сортов кукурузы. Однако перегрев зерна в чане создает опасность клейстеризации крахмала и заваривания зерна.
При выдерживании на требуемом уровне всех показателей режима замачивания зерна его продолжительность в пределах 32-50 часов является оптимальной при переработке кукурузы на крахмал. Исследователи ищут способы дальнейшего сокращения длительности этого процесса. Результаты опытов по сокращению времени замачивания зерна до 32-36 часов показали, что выход крахмала в производстве не снижается, зерно перерабатывается легко. При этом наблюдается некоторое снижение выхода экстракта, что закономерно, так как уменьшается время перехода нерастворимых веществ зерна в растворимое состояние. Удлинение периода замачивания кремнистых сортов кукурузы тоже не приводит к существенному возрастанию выхода крахмала. Иногда увеличивают продолжительность замачивания, чтобы компенсировать недостаточную температуру процесса, или концентрацию сернистого газа. Однако такой путь неэффективен. На практике сернистая кислота обычно подается на замоченное зерно и движется противотоком к свежезагруженному. При этом концентрация ее уменьшается, и свежезагруженное зерно длительное время сохраняет неденатурированные клетки, что ухудшает диффузию из них растворимых веществ (рис.5.9). Если кислота подается сначала на свежезагруженное зерно, это значительно ускоряет процесс денатурации. Затем из этого чана она возвращается в чан, предшествующий промывке, и движется в батарее, как обычно. Такой способ получил название "петлевого". Он позволяет на несколько часов сократить продолжительность замачивания без существенных затрат
Рис. 5.10. Схема станции непрерывного замачивания зерна кукурузы
Периодический способ замачивания зерна в чанах, объединенных в замочную батарею, имеет ряд недостатков. Так как весь комплекс технологических операций - загрузка зерна, откачивание экстракта, замачивание, подача сернистой кислоты, промывание и выгрузка зерна осуществляется в каждом чане батареи, то все они должны быть снабжены необходимым оборудованием, трубопроводами и запорной арматурой. Емкости замочных чанов при выгрузке и загрузке зерна используются не полностью, на обслуживание станции идут большие затраты ручного труда. С применением способа непрерывного замачивания зерна значительно упрощается устройство станции замачивания, так как каждая часть ее выполняет только определенные технологические функции. В нашей стране получила распространение установка непрерывного замачивания зерна, в которой используются отдельные чаны традиционной станции (рис. 5.10). Число замочных чанов в установке позволяет выдерживать определенную длительность и кратность технологических процессов — промывания и диффундирования растворимых веществ. Замачивание зерна ведется методом противотока в замочных батареях, состоящих из чанов, оснащенных насосами для перекачки зерна и ситовым устройством для отделения и подогрева замочной воды в трубчатом теплообменнике. Но наиболее эффективным считается эрлифтный способ перекачивания водно-зерновой смеси, при котором зерно не повреждается и более равномерно перемешивается.
Щелочной способ замачивания зерна и продуктов его размолаЗерновые и зернобобовые культуры значительно различаются по составу белковых веществ. В пшенице, ржи, ячмене и рисе преобладают щелочнорастворимые белки, в связи с чем для размягчения зерна применяют щелочной способ его обработки. Белки зерновых культур представляют собой амфотерные соединения, так как они содержат и карбоксильную группу - СООН, и основную - NН2:
NH3OH NH3OH
COOH COONa
При диссоциации соли в воде образуются ионы:
NH3OH NH3OH - + R + NaOH R + Na COONa COO
Знак заряда их в растворе зависит от концентрации водородных ионов раствора. Коллоидная частица белка К., реагируя со щелочью, например, с едким натрием, образует соль белка. Таким образом, белковые частицы в щелочном растворе заряжены отрицательно, а в кислой среде они несут положительный заряд. Щелочной способ замачивания целого зерна кукурузы, пшеницы, ржи, ячменя и гороха применяется редко - как вынужденная мера для загрузки картофелекрахмальных заводов в межсезонный период. Для этой цели используются продукты размола зерна этих культур в виде муки разной степени помола. При таком способе замачивания клейковинные белки (глиадин и глютенин) разрушаются полностью, и клейковина в качестве готового продукта не выделяется. В связи с этим щелочной способ замачивания пшеничной муки применяется только для зерна пшеницы мягких сортов с низким содержанием клейковины. Параметры технологического процесса замачивания щелочным способом ржаной муки предложены во ВНИИ крахмалопродуктов Е.А. Штырковой. Ржаномучная суспензия обрабатывается щелочным раствором концентрацией 0,25% при поддержании оптимальной величины рН на уровне 11-11,3 и активно перемешивается при температуре 30°С. При таком режиме удаётся разрушить до 95% белков и пентозанов и снизить вязкость суспензии до 5 мПа-с. Общая концентрация сухих веществ в суспензии 7 - 8%, что создает проблему утилизации этих сильноразбавленных белковых отходов. Составные части зерна гороха поразному реагируют на условия и параметры обработки при замачивании - температуру, продолжительность, присутствие химических реагентов. Замачивание зерна гороха осуществляется в 0,05 н растворе щелочи при гидромодуле 1:2,5, температуре 40...45 °С следующим образом: замочный раствор с рН 11-11,5 подается в чан, в который уже загружено зерно, затем подогревается путем рециркуляции "на себя" замочной воды циркуляционными насосами через подогреватель типа "труба в трубе". Аналогично готовят загрузку второго чана: наполняют его зерном, заливают замочным реагентом, осуществляют его рециркуляцию и т.д. По окончании замачивания зерно вместе с замочной водой, имеющей рН 8,5 - 9,0, насосом транспортируется на отцеживающее сито перед измельчением. Такая предварительная подготовка зерна гороха с избирательным разрушением его структуры обеспечивает коэффициент извлечения крахмала 85 - 90, экстракта - 10 - 12, белка - 12 - 13% СВ. Химический состав сгущенного горохового экстракта, %: сухие вещества - 48,2, протеин - 8, небелковые азотистые вещества - 5,61, редуцирующие вещества - 16,6, зола - 8,3. Особенности щелочного замачивания риса.По старинному способу О.Jones [101], рис замачивают в течение 24 ч в 5-кратном количестве (по массе) раствора каустической соды, приготовленного в соотношении - 1 часть каустической соды на 350 частей воды. Затем раствор удаляют, и зерно промывают избыточным количеством воды при сильном перемешивании. Освобожденный от воды рис измельчают в истирающей мельнице; полученную массу размешивают в 10-кратном количестве раствора каустической соды в течение ~ 24 ч, затем крахмал осаждают в течение 20 ч. Основная часть белковых веществ переходит в надосадочный слой щелочного раствора, который тщательно отделяют декантацией. Крахмал вновь суспендируют в 20-кратном количестве воды и энергично перемешивают. Разбавленную крахмальную суспензию процеживают для отделения взвешенных примесей. Промывку, осаждение, декантацию повторяют, и чистую крахмальную суспензию направляют на осаждение. Замачивание в щелочи зачастую проводят в емкостях с перфорированным дном, и раствор щелочи рециркулирует через массу риса. Отделение крахмала от воды и щелочи производят центрифугированием. Щелочной замачивающий раствор используют многократно, подогревая его перед замачиванием до 44...54 °С. Во ВНИИ крахмалопродуктов проведены исследования щелочного способа замачивания и измельчения рисовой крупки, по результатам которых (табл.5.1) А.И. Жушманом и Н.И. Филипповой предложена новая технология рисового крахмала.
Таблица 5.1 Характеристика продуктов, получаемых при переработке рисовой крупки на крахмал щелочным способом, % СВ
Технологическая схема включает следующие операции: замачивание рисовой крупки при температуре 48...50°С в течение 4ч в 0,4%-ном растворе едкого натра; отделение экстракта от крупки на центрифуге типа ОГШ; промывание и измельчение крупки на машине ударного типа; повторное замачивание измельченной кашки в щелочном растворе той же концентрации; отделение экстракта на центрифуге; отделение мезги на ситовых аппаратах с сеткой №67; однократная обработка крахмало-белковой суспензии на шнековой центрифуге НОГШ-325н; механическое обезвоживание крахмала на осадочной центрифуге; сушка и рассев крахмала. В промышленных условиях выход крахмала из переработанной рисовой дробленки составил 54,5% СВ при содержании протеина в крахмале не более 1,0%.
5.4.3.2. Комбинированные способы замачивания зернового сырья
На практике использование для избирательного разрушения структуры крахмалсодержащего сырья только одного способа замачивания встречается редко. Как правило, применяется комплексная обработка сырья. В этом отношении наиболее характерен процесс замачивания зерна ячменя. Одними из основных технологических операций при получении ячменного крахмала являются отделение пленок от сухого зерна и его замачивание в растворах щелочи или сернистой кислоты. Во ВНИИ крахмалопродуктов проведены испытания для определения влияния шелушения зерна ячменя на изменение его структуры при замачивании с различными реагентами и в чистой воде (табл. 5.2) [31]. Таблица 5.2 Сравнительные данные по качеству замачивания необрушенного и обрушенного зерна ячменя с разными реагентами
При замачивании в любом из выбранных реагентов основное количество влаги целое зерно ячменя поглощает в первые 24 ч. Степень набухания при использовании раствора сернистой кислоты достигает максимума после 24 ч, воды - после 36 ч, а щелочи - продолжает возрастать и после 36 ч. При этом наименьшее количество влаги поглощается зерном при замачивании в растворах Н2SОз, наибольшее - в щелочи. Наиболее полно и быстро растворимые вещества зерна ячменя переходят в замочную воду при замачивании в растворах сернистой кислоты; скорость их перехода при использовании воды - значительно меньше. При замачивании зерна ячменя в растворе щелочи растворимые вещества в зерне практически не изменяются после 24 ч. С увеличением температуры от 0 до 48°С возрастает степень набухания зерна и повышается выход экстрактивных веществ. При более продолжительном замачивании (до определенного предела) и увеличении температуры снижаются потери крахмала, связанного с мезгой, а выход его возрастает. При замачивании обрушенного зерна ячменя содержание в нем растворимых веществ ниже, а выход экстракта значительно выше, чем для необрушенного. Один из основных способов комбинирования переработки зернового сырья на картофелекрахмальных заводах в межсезонный период с использованием для замачивания зерна едкого натра (щелочной способ) или пиросульфита натрия (сернистокислотный способ) - подробно описан в разделе 8.2. Биологическая обработка зернового сырья при замачиванииэффективна только при определенной кислотности замочной воды, что достигается применением химических реагентов соответствующей концентрации, а также предварительным дроблением зерна или измельчением его вплоть до муки. Так, при совместном воздействии пиросульфита натрия и целлюлолитических ферментов на пшенично- и ржано-мучную суспензии при замачивании резко снижается их вязкость и соответственно возрастает коэффициент извлечения крахмала, что обусловлено одновременным разрушением белковой матрицы и образующихся при этом комплексов некрахмальных полисахаридов (пентозанов) с растворимыми белками. Анализ многообразных способов предварительного разрушения структуры крахмалсодержащего сырья, в основном зерна, открывает большие возможности для эффективного ведения технологического процесса извлечения крахмала путем выбора наиболее рационального способа и оптимальных режимов подготовки сырья и дальнейшего совершенствования этих технологических операций.
Механо-гидравлические способы разрушения структуры сырья.Для полного разрушения структуры сырья и разрыва связей зерен крахмала с другими его компонентами используются различные способы измельчения зерен и корнеклубнеплодов. Наиболее древний, истирающий, способ сохранился и в наши дни. Он ведет свое начало от ручных жерновов для зернового сырья и тёрок для корнеклубнеплодов. С переходом на промышленную выработку крахмала и необходимостью в связи с этим увеличения производительности оборудования был осуществлен его машинный привод, а сами конструкции жерновов и терок подверглись существенному совершенствованию. К основным недостаткам данного способа относятся высокая степень переизмельчения компонентов сырья, недостаточное отделение от них зерен крахмала из-за большого диапазона их размеров (3 - 100 мкм). До такой же степени измельчаются остальные компоненты сырья, хотя в этом нет необходимости. В последние десятилетия истирающий способ измельчения крахмалсодержащего сырья постепенно вытесняется ударным и ударно-истирающим способами. Они обеспечивают избирательное разрушение структуры сырья с высвобождением зерен крахмала и минимальным разрушением оболочек, волокон и других его структурообразователей. Преимущество ударного способа измельчения заключается в том, что частицы крахмалсодержащего сырья могут вести себя как пакеты, наполненные суспензией. При ударе их о жесткую поверхность оболочки разрываются, освобождая содержимое при минимальном разрушении самих оболочек [4, 38]. К разновидностям ударного способа измельчения относятся: - разгон и удар частиц о жесткое препятствие; - самоизмельчение при соударении кусков и частиц измельчаемого материала; - кавитационное измельчение материалов в жидкости посредством возбуждения гидравлических ударов [3, 4, 40, 59,80] . Ударный способ измельчения наиболее широко применяется для разрушения хрупких материалов. В последнее время он стал использоваться и для воздействия на упруго-пластичные и упруго-вязкие материалы, так как при высоких скоростях их нагружения пластические и вязкие деформации не успевают развиться, и их разрушение носит характер разрушения хрупкого тела. Зерновые виды крахмалсодержащего сырья относятся к упруго-пластичным материалам, а корнеклубнеплоды - к упруго-вязким, но при соответствующей обработке зерно приобретает также и упруго-вязкие свойства. Скорость удара, при которой начинается разрушение частиц, хотя и определяет необходимую скорость рабочих органов ударных измельчителей, однако фактические скорости их гораздо выше расчетных, так как условия прямого центрального удара не могут быть обеспечены для всех частиц. Кроме того, осколки частиц, полученные при разрушении, должны иметь достаточную скорость, чтобы покинуть зону измельчения. Необходимость увеличения скорости рабочих органов ударных измельчителей обосновывается следующими основными положениями:
Возникшее противоречие в теории ударного измельчения между повышением к.п.д. ударного способа измельчения при увеличении скорости удара и падением к.п.д. измельчителя из-за возрастания гидравлических потерь на трение рабочих органов разрешается путем применения - в основном для хрупких материалов с упругими свойствами - ударных измельчителей без движущихся рабочих органов с использованием принципа самоизмельчения, который для упруго-вязких и упруго-пластичных материалов неэффективен. В связи с этим для таких материалов применяется многоступенчатый ударный способ измельчения при сравнительно невысокой скорости рабочих органов измельчителей. Задача определения необходимого числа приемов разрушения п решается с использованием метода Стедлера с учетом увеличения степени однократного разрушения при превышении критической скорости удара. Так, по Стедлеру, число необходимых приемов разрушения п определяется соотношением исходного с10 и конечного с1„ размеров частицы:
Кавитационный способ тонкого измельчения крахмалсодержащего сырья.
К ударному способу измельчения относится также кавитационный. Он основан на многократном резком перепаде давления жидкости, сопровождающей продукт. При понижении давления происходит вскипание и образование пузырьков; при его повышении они лопаются с возникновением гидравлических ударов. Измельчение кавитацией осуществляется в три этапа. Вначале, когда лопаются полусферические кавитационные пузырьки, образуется кумулятивная струйка, создающая на поверхности продукта микроизьяны (рис. 5.18) [40,47]. Струйка воздействует на продукт с давлением Р = 8 108-1010 Па. В дальнейшем пузырек воздействует на измельчаемый материал посредством расклинивающей силы Бьеркнесса, которая расширяет полученные на предыдущем этапе микроизьяны и природные царапины до полного разрушения частицы на две и более части.
Рис. 5.18. Схема действия кавитационных пузырьков по разрушению частицы твердого тела
Под воздействием ударных волн, возникающих при схлопывании кавитационного пузырька, в жидкости образуются импульсы давления Р = 3*107 Па и происходит последующее измельчение продукта. Кавитационный эффект в жидкости может быть создан различными способами. Самый распространенный и нежелательный эффект кавитации возникает в центробежных насосах при разрыве струи в разгонной проточной их части. Этот принцип и был использован в дальнейшем для конструирования кавитационных мельниц и диспергаторов, которые получили широкое распространение в пищевой индустрии. Однако при тонком измельчении мучных суспензий диспергаторами такого типа не обеспечивается полное отделение белковых частиц от зерен крахмала. В последние годы для тонкого измельчения водных пшеничномучных суспензий стали широко применяться насосы высокого давления с гомогенизирующей головкой (рис. 5.19).
Принцип работы гомогенизатора заключается в следующем: мучная суспензия прокачивается через вибрирующий клапан с перепадом давления до 15 Мпа; при этом образующиеся и захлопывающиеся в щели клапана кавитационные пузырьки воздействуют на крупные частицы муки, разрывают их и высвобождают зерна крахмала. Впервые гомогенизатор для тонкого измельчения кукурузной кашки применили Р.Меизег и Н.Низ1ег. При этом гомогенизация кашки осуществлялась в четыре стадии. Оценка качества измельчения после каждой из них проводилась по изменению размера частиц и содержанию крахмала в мезге [80]. Характер разрушения клетчатки гомогенизирующей головки [801: отражен на микрофотографиях (рис.5.20), где отчетливо видны пустые клетки, из которых высвобождены зерна крахмала. Размеры частиц кукурузной кашки после гомогенизатора уменьшаются во всех фракциях более чем в два раза при полном отсутствии частиц более 500 мкм .
После первой стадии гомогенизации основную долю составляют частицы размерами 160-500 мкм, а после двух стадий - 63-160 мкм. Основное преимущество гомогенизатора состояло не только н дополнительном высвобождении крахмальных зерен из клетчатки, но также в отделении их от белковых частиц и снижении вязкости кукурузной кашки, которая становится разделяемой. В табл. 5.4 наглядно отражены результат осаждения крахмала в кукурузной кашки после гомогенизации, полученные на лабораторной центрифуге. Таблица 5.4 Разделение кукурузной кашки - до и после Гомогенизации
Литература Lit1.JPG, Lit2.JPG, Lit3.JPG, Lit4.JPG, Lit5.JPG, Lit6.JPG, Lin7.JPG
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||